
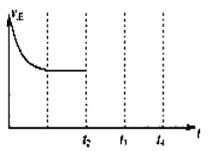
 2013年9月,中國華北華中地區發生了嚴重的霧霆天氣,北京、河北、河南等地的空氣污染升為6級空氣污染,屬于重度污染.汽車尾氣、燃煤廢氣、冬季取暖排放的CO2等都是霧霆形成的原因.
2013年9月,中國華北華中地區發生了嚴重的霧霆天氣,北京、河北、河南等地的空氣污染升為6級空氣污染,屬于重度污染.汽車尾氣、燃煤廢氣、冬季取暖排放的CO2等都是霧霆形成的原因.| 催化劑 |
| 實驗組 | 溫度 ℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
| m |
| V |
| m |
| n |
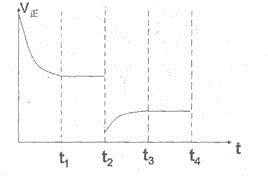 ,故答案為:
,故答案為: ;
;| c(CO2)c(H2) |
| c(H2O)c(CO) |
| 0.8×0.8 |
| 0.2×1.2 |
| 1.6 |
| 4 |
| 0.4 |
| 2 |


科目:高中化學 來源: 題型:
 如表為元素周期表前四周期的一部分,下列有關R、W、X、Y、Z五種元素的敘述中,正確的是( )
如表為元素周期表前四周期的一部分,下列有關R、W、X、Y、Z五種元素的敘述中,正確的是( )| A、原子半徑:X>W>Y |
| B、Y、Z的陰離子電子層結構都與R原子的相同 |
| C、W的氫化物比X的氫化物穩定 |
| D、Y元素的最高價氧化物對應水化物比W元素的最高價氧化物對應水化物的酸性強 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、NaHSO4溶液與Ba(OH)2溶液混合后溶液呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | ||||
| B、將標準狀況下112 mL氯氣通入10 mL 1 mol?L-1的溴化亞鐵溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 | ||||
C、用惰性電極電解飽和MgCl2溶液:2Cl-+2H2O
| ||||
| D、向澄清石灰水中加入過量的碳酸氫鈉溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、用已知濃度的鹽酸滴定未知濃度的氫氧化鈉溶液時,讀取滴定管末讀數時,仰視刻度線 |
| B、測定硫酸銅晶體中結晶水含量的實驗時,加熱時間過短未完全變白 |
| C、中和滴定時,加待測液前錐形瓶內有少量水 |
| D、測定1mol氫氣體積的操作中,反應結束后未抽氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| n |
| 2 |
| 3n |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
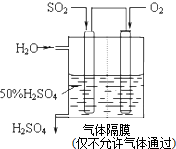
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
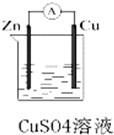 某化學興趣小組利用如圖所示原電池裝置進行實驗,請回答下列問題:
某化學興趣小組利用如圖所示原電池裝置進行實驗,請回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com