
| A. | .電池工作時,MnO2發生還原反應 | |
| B. | .電池負極的電極反應式為:2MnO2+H2O+2e-→Mn2O3+2OH- | |
| C. | .電池工作時,電路中每通過0.2mol電子,鋅的質量理論上減少6.5g | |
| D. | 電池工作時,K+移向負極 |
分析 根據電池總反應式為:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s),可知反應中Zn被氧化,為原電池的負極,負極反應為Zn-2e-+2OH-═Zn(OH)2,MnO2為原電池的正極,發生還原反應,正極反應為2MnO2(s)+H2O(1)+2e-═Mn2O3(s)+2OH-(aq),以此解答該題.
解答 解:A.根據總反應可知,MnO2中Mn元素的化合價降低,發生還原反應,故A正確;
B.負極Zn失電子,發生氧化反應,所以負極的電極反應式為:Zn-2e-+2OH-=Zn(OH)2,故B錯誤;
C.由Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s)可知,65gZn反應轉移電子為2mol,則6.5gZn反應轉移0.2mol電子,故C正確;
D.電池工作時,電子由負極流向正極,根據異性電荷相吸,溶液中K+、H+向正極移動,OH-向負極移動,故D錯誤.
故選AC.
點評 本題考查化學電源的工作原理,題目難度不大,注意電極反應方程式的書寫和原電池正負極的判斷.理解這類題的關鍵是理解原電池原理,在反應中,電子從負極經外電路流向正極,同時溶液中的陰、陽離子分別不斷移向負極、正極,構成閉合回路.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 金剛石比石墨穩定 | |
| B. | 1 mol石墨所具有的能量比1 mol金剛石低 | |
| C. | 金剛石轉變成石墨是物理變化 | |
| D. | 石墨和金剛石都是碳的同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 1mol H2O 分解為H2與O2需吸收930 kJ熱量 | |
| B. | H與O反應生成1mol H2O放出930 kJ熱量 | |
| C. | 2 mol H的能量小于1mol H2的能量 | |
| D. | H結合成H2放出436 kJ的熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “海水淡化”可以解決“淡水供應危機”,向海水中加入凈水劑明礬可以使海水淡化 | |
| B. | 食用油和人造奶油都是油酸甘油酯 | |
| C. | 只要符合限量,“食用色素”、“亞硝酸鹽”可以作為某些食品的添加劑 | |
| D. | 雞蛋清中加入膽礬可以使蛋白質發生鹽析 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
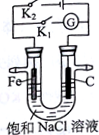 如圖所示,將鐵棒和石墨棒插入盛有飽和NaCl溶液的U型管中.下列敘述正確的是( )
如圖所示,將鐵棒和石墨棒插入盛有飽和NaCl溶液的U型管中.下列敘述正確的是( )| A. | K1閉合,向鐵棒附近滴入K3[Fe(CN)6]溶液,有藍色沉淀出現 | |
| B. | K1閉合,電流方向由鐵棒經導線流向石墨棒 | |
| C. | K2閉合,碳棒是陰極 | |
| D. | K2閉合,電路中通過0.2NA個電子時,兩極共產生4.48L氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O→NaOH | B. | NaHCO3→Na2CO3 | C. | SiO2→H2SiO3 | D. | NH3→NO |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
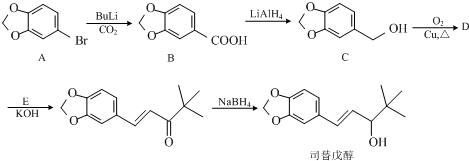
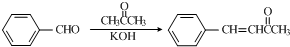
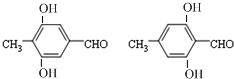 (任意一種);.
(任意一種);.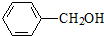 為原料制備
為原料制備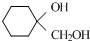 的反應合成路線流程圖(無機試劑任用).
的反應合成路線流程圖(無機試劑任用).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HC1 | B. | 2CH3CH2OH+02$\stackrel{Cu、△}{→}$2CH3CH0+2H20 | ||
| C. | 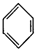 +HNO3$→_{50-60℃}^{濃硫酸}$ +HNO3$→_{50-60℃}^{濃硫酸}$ +H2O +H2O | D. | nCH2=CH2$\stackrel{一定條件}{→}$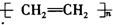 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com