
| A. | Na+、Mg2+、Cl-、SO42- | B. | Cu2+、Cl-、NO3-、OH- | ||
| C. | Ca2+、Na+、CO32-、NO3- | D. | K+、Fe3+、NO3-、SCN- |
分析 A.四種離子之間不反應,能夠共存;
B.鐵離子與氫氧根離子反應生成氫氧化銅沉淀;
C.鈣離子與碳酸根離子反應生成碳酸鈣沉淀;
D.鐵離子與硫氰根離子反應生成硫氰化鐵.
解答 解:A.Na+、Mg2+、Cl-、SO42-之間不發生反應,在溶液中能夠大量共存,故A正確;
B.Cu2+、OH之間反應生成難溶物氫氧化銅,在溶液中不能大量共存,故B錯誤;
C.Ca2+、CO32-之間反應生成難溶物碳酸鈣,在溶液中不能大量共存,故C錯誤;
D.Fe3+、SCN-之間發生絡合反應,在溶液中不能大量共存,故D錯誤;
故選A.
點評 本題考查離子共存的判斷,題目難度不大,注意掌握離子反應發生條件,明確離子不能大量共存的一般情況:能發生復分解反應的離子之間;能發生氧化還原反應的離子之間;能發生絡合反應的離子之間(如 Fe3+和 SCN-)等;試題側重對學生基礎知識的訓練和檢驗,有利于培養學生的邏輯推理能力,提高學生靈活運用基礎知識解決實際問題的能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:多選題
| A. | Fe做還原劑 | B. | FeO做氧化劑 | ||
| C. | 鐵元素的化合價降低 | D. | 鐵元素化合劑升高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 它可能能使酸性高錳酸鉀溶液褪色 | |
| B. | 一氯代物可能只有一種 | |
| C. | 分子結構中甲基的數目可能是0、1、2 | |
| D. | 等質量CH4和C4H8分別在氧氣中完全燃燒,CH4的耗氧量小于C4H8 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題

| A. | 溶液的pH=9時,溶液中存在下列關系:c(HCO3-)>c(NH4+)>c(NH3•H2O)>c(CO32-) | |
| B. | NH4HCO3溶液中存在下列守恒關系:c(NH4+)+c(NH3•H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| C. | 由圖可知,往該溶液中逐滴滴加氫氧化鈉時NH4+和HCO3-濃度逐漸減小 | |
| D. | 通過分析可知常溫下Ka1(H2CO3)>Kb(NH3•H2O)>Ka2(H2CO3) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
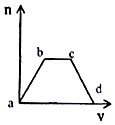 將足量CO2通入KOH和Ca(OH)2的混合溶液中,生成沉淀的質量(m)和通入CO2體積(V)的關系如圖所示:
將足量CO2通入KOH和Ca(OH)2的混合溶液中,生成沉淀的質量(m)和通入CO2體積(V)的關系如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
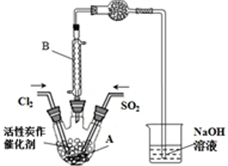 已知:SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H=-a kJ•mol-1
已知:SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H=-a kJ•mol-1| SO2Cl2 | Cl2 | SO2 | |
| 熔點/℃ | -54.1 | -101 | -72.4 |
| 沸點/℃ | 69.1 | -34.6 | -10 |
| 性質 | 遇水發生劇烈水解 | / | / |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 ;與E同周期的元素中,金屬性最弱的金屬元素名稱是鋁,最穩定的氣態氫化物的化學式為HCl;
;與E同周期的元素中,金屬性最弱的金屬元素名稱是鋁,最穩定的氣態氫化物的化學式為HCl; ,B與D通常能形成共價(填“離子”或“共價”)化合物,在E2D2中含有的化學鍵有離子鍵、非極性共價鍵.
,B與D通常能形成共價(填“離子”或“共價”)化合物,在E2D2中含有的化學鍵有離子鍵、非極性共價鍵.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com