
| A. | NaClO溶液中通入少量SO2:ClO-+SO2+H2O=2H++SO42-+Cl- | |
| B. | FeCl3溶液中通入過量H2S氣體:2Fe3++3H2S=2FeS↓+S↓+6H+ | |
| C. | Na2CO3溶液中通入少量Cl2:2CO32-+Cl2+H2O=ClO-+Cl-+2HCO3- | |
| D. | NaHSO3溶液中通入少量Cl2:HSO3-+Cl2+H2O=3H++SO42-+2Cl- |
分析 A.發生氧化還原反應生成硫酸鈉、氯化鈉,堿性溶液中不能生成H+;
B.FeS溶于酸;
C.反應生成氯化鈉、次氯酸鈉、碳酸氫鈉;
D.發生氧化還原反應,氯氣不足還生成二氧化硫.
解答 解:A.NaClO溶液中通入少量的SO2的離子反應為ClO-+2OH-+SO2═Cl-+SO42-+H2O,故A錯誤;
B.FeCl3溶液中通入過量H2S氣體的離子反應為2Fe3++H2S=2Fe2++S↓+2H+,故B錯誤;
C.Na2CO3溶液中通入少量Cl2的離子反應為2CO32-+Cl2+H2O=ClO-+Cl-+2HCO3-,故C正確;
D.NaHSO3溶液中通入少量Cl2的離子離子反應為4HSO3-+Cl2=3H2O+3SO2↑+SO42-+2Cl-,故D錯誤;
故選C.
點評 本題考查離子反應方程式書寫的正誤判斷,為高頻考點,把握發生的反應及離子反應的書寫方法為解答的關鍵,側重氧化還原反應的離子反應考查,題目難度較大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | A的平均消耗速率為0.32mol•L-1•min-1 | |
| B. | B的轉化率為80% | |
| C. | x的值為2 | |
| D. | B的平衡濃度為1mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
. .
. +2OH-$\stackrel{△}{→}$
+2OH-$\stackrel{△}{→}$ +CH3OH+H2O.
+CH3OH+H2O. ,該反應類型是縮聚.
,該反應類型是縮聚. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  向里推活塞時,長頸漏斗中有一段水柱,靜止,水柱高度不變 該裝置的氣密性良好 向里推活塞時,長頸漏斗中有一段水柱,靜止,水柱高度不變 該裝置的氣密性良好 | |
| B. |  脫脂棉燃燒 Na2O2與水反應生成氫氧化鈉和氧氣 脫脂棉燃燒 Na2O2與水反應生成氫氧化鈉和氧氣 | |
| C. |  燒杯①的澄清石灰水先變渾濁 NaHCO3比Na2CO3受熱更易分解 燒杯①的澄清石灰水先變渾濁 NaHCO3比Na2CO3受熱更易分解 | |
| D. |  U形管右端的液面高 鐵釘發生吸氧腐蝕 U形管右端的液面高 鐵釘發生吸氧腐蝕 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 ?
?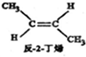 ,△H=-4.2kJ.mol-1
,△H=-4.2kJ.mol-1 (g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.
(g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.| A. | 反-2-丁烯比順-2-丁烯穩定 | |
| B. | 順-2-丁烯的燃燒熱數值比反-2-丁烯小 | |
| C. | 減壓和升溫有利于平衡向生成正丁烷反應方向移動 | |
| D. | 反-2-丁烯氫化的熱化學方程式為: (g)+H2(g)?CH3CH2CH2CH3(g),△H=-123.1kJ•mol-1 (g)+H2(g)?CH3CH2CH2CH3(g),△H=-123.1kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Na+、H+、C1- | B. | Na+、Ba2+、Mg2+、NO3- | ||
| C. | NH4+、K+、Cl-、NO3- | D. | K+、Na+、CO32-、S2- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不溶于水,且必須易與碘發生化學反應 | |
| B. | 不溶于水,不與碘發生化學反應且比水更易溶解碘 | |
| C. | 不溶于水,且必須比水密度大 | |
| D. | 不溶于水,且必須比水密度小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com