
| A. | 一定溫度下,10mL 0.50mol•L-1NH4Cl溶液與20mL 0.25mol•L-1NH4C1溶液含NH4+物質的量相同 | |
| B. | 25℃時,將a mo1•L-l氨水與0.01 moI•L-1鹽酸等體積混合,反應完全時溶液中c(NH4+)=c(C1-),用含a的代數式表示反應完全時NH3•H2O的電離常數Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
| C. | 一定溫度下,已知0.1 mol•L-1 的醋酸溶液中存在電離平衡:CH3COOH?CH3COO-+H+,加少量燒堿溶液可使溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$值增大 | |
| D. | 等體積、pH都為3的酸HA和HB分別與足量的鋅反應,HA放出的氫氣多,說明酸性:HA>HB |
分析 A、銨根離子水溶液中水解,濃度不同水解程度不同分析;
B、當溶液中c(NH4+)=c(C1-),說明溶液呈中性,有c(H+)=c(OH-)=10-7,NH3•H2O的電離平衡常數Kb=$\frac{c(N{{H}_{4}}^{+})•c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$;
C、要使溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$值增大,應是平衡向電離的方向移動,結合影響平衡移動的因素解答該題;
D、等體積等PH值的酸,酸的濃度越大,酸性越弱.
解答 解:A、NH4Cl 濃度越小,NH4+水解程度越大,不考慮水解1L 0.50mol•L-1NH4Cl 溶液與2L 0.25mol•L-1 NH4Cl 溶液銨根的物質的量相同,但0.25mol•L-1NH4Cl 溶液中銨根水解程度大,所以含NH4+ 物質的量前者大,故A錯誤;
B、當溶液中c(NH4+)=c(C1-),說明溶液呈中性,有c(H+)=c(OH-)=10-7,故NH3•H2O的電離平衡常數Kb=$\frac{c(N{{H}_{4}}^{+})•c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{0.005×1{0}^{-7}}{0.5(a-0.01)}$=$\frac{1{0}^{-9}}{a-0.01}$,故B正確;
C、加入少量燒堿溶液,反應生成CH3COO-,c(H+)減小,由于CH3COO-對CH3COOH的電離起到抑制作用,則$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$值減小,故C錯誤;
D、當體積、pH都為3的酸HA和HB分別與足量的鋅反應,HA放出的氫氣多,說明HA的物質的量大于HB的物質的量,溶液的體積相等,HA的物質的量濃度大于HB的,所以說明酸性:HA<HB,故D錯誤;
故選B.
點評 本題考查了鹽類水解程度大小的影響因素、電離平衡常數的計算、弱酸的電離平衡移動、pH相等的酸,酸性越弱其濃度越大,題目難度不大.


 陽光試卷單元測試卷系列答案
陽光試卷單元測試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | pH=13 | |
| B. | pH=2 | |
| C. | 由水電離出的c(H+)=0.01 mol/L | |
| D. | 溶質的物質的量濃度為0.005 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 著色劑---胡蘿卜素、苯甲酸鈉 | B. | 調味劑---亞硝酸鈉、味精 | ||
| C. | 防腐劑---氯化鈉、檸檬黃 | D. | 營養強化劑---醬油中加鐵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
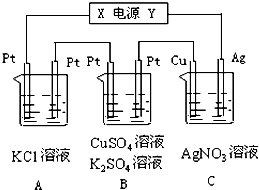 如圖所示,若電解5min時銅電極質量增加2.16g,試回答:
如圖所示,若電解5min時銅電極質量增加2.16g,試回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化碳和甲烷均是造成溫室效應的氣體 | |
| B. | 可借助于核磁共振氫譜區分乙醇和二甲醚這兩種物質 | |
| C. | 漂白液的有效成分是NaClO,制作計算機芯片的材料是SiO2晶體 | |
| D. | 食醋可去除水垢,NH4Cl溶液可去除鐵銹 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 非金屬元素間形成的化學鍵都是共價鍵 | |
| B. | 第三周期主族元素的最高正化合價等于它所處的族序數 | |
| C. | 短周期元素形成離子后,最外層都達到8電子穩定結構 | |
| D. | 最外層電子數相同的原子屬于同一族且化學性質相似 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 陰極:NaOH溶液質量分數 | 陽極:NaCl溶液濃度(g/L) | |
| 進料液 | 0.30 | 310 |
| 電解后 | 0.32 | 210 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com