
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反應前2min的平均速率ν(Z)=2.0×10-5 mol/(L•min) | |
| B. | 4min時,ν(逆)>ν(正) | |
| C. | 該溫度下,此反應的平衡常數K=1.44 | |
| D. | 7min時,反應還未達到平衡狀態 |
分析 A、2min內Y物質的量變化為0.16mol-0.12mol=0.04mol,求出Z的物質的量變化,根據v=$\frac{\frac{△n}{V}}{△t}$計算v(Z);
B、根據4min時的濃度變化分析,反應進行到7minY的物質的量減小,說明反應正向進行;
C、由表中數據可知7min時,反應到達平衡,根據平衡時Y的物質的量,利用三段式計算平衡時其它組分的物質的量,由于反應氣體氫氣的化學計量數相等,用物質的量代替濃度代入平衡常數表達式計算;
D、數據分析可知7min,到9min,Y的物質的量不變,說明此時反應已達到平衡狀態.
解答 解:A、由表中數據可求得2min內Y物質的量變化為0.16mol-0.12mol=0.04mol,則前2min內生成Z為0.08mol,故v(Z)=$\frac{\frac{0.08mol}{10L}}{2min}$=4×10-3mol/(L•min),故A錯誤;
B、4min時,n(Y)=0.11mol,7min時n(Y)=0.10mol,是說明隨時間增長,Y的物質的量減小,說明反應正向進行,ν(逆)<ν(正),故B錯誤;
C、由表中數據可知7min時,反應到達平衡,Y的物質的量為0.10mol,此時X的物質的量也為0.10mol,Z的物質的量也為0.12mol,X、Y、Z的物質的量濃度分別為:0.01mol•L-1、0.01mol•L-1、0.012mol•L-1,故平衡常數K=$\frac{{c}^{2}(Z)}{c(X)c(Y)}$=$\frac{0.01{2}^{2}}{0.01×0.01}$=1.44,故C正確;
D、數據分析可知7min到9min,Y的物質的量不變,說明7min時,反應已達到平衡狀態,故D錯誤.
故選C.
點評 本題考查化學反應速率、化學平衡常數、化學平衡的影響因素等,難度中等,注意C選項中對化學平衡常數的理解.


科目:高中化學 來源: 題型:選擇題
| A. | 9gH2O中含有NA個電子 | |
| B. | 標準狀況下,22.4L乙醇中含有2NA個碳原子 | |
| C. | 25℃,0.2mol•L-1CH3COONa溶液含有0.2NA個CH3COO- | |
| D. | 2.4g鎂在空氣中充分燃燒生成MgO和Mg3N2,轉移0.2NA個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 鐵、鋁、銅及其化合物在生產、生活中有著廣泛的應用.請回答下列問題:
鐵、鋁、銅及其化合物在生產、生活中有著廣泛的應用.請回答下列問題: .
.| 選項 | 陳述Ⅰ | 陳述Ⅱ | 判斷 |
| A | 鐵是地殼中含量最高的金屬元素 | 鐵是人類最早使用的金屬材料 | Ⅰ對;Ⅱ對. |
| B | 常溫下鐵與稀硫酸反應生成氫氣 | 高溫下氫氣能還原氧化鐵生成鐵 | Ⅰ對;Ⅱ對. |
| C | 鐵比鋁更易銹蝕 | 鋁比鐵活潑 | Ⅰ錯;Ⅱ對. |
| D | 鋁在空氣中表面生成致密氧化膜 | 可用鋁罐儲存運輸濃硫酸、濃硝酸 | Ⅰ錯;Ⅱ對. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用催化劑 | B. | 增大A物質的濃度 | C. | 增大B物質的濃度 | D. | 減少C物質的濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
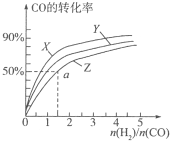 甲醇是重要的燃料,有廣闊的應用前景:工業上一般以CO和為原料合成甲醇,該反應的熱化學方程式為:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
甲醇是重要的燃料,有廣闊的應用前景:工業上一般以CO和為原料合成甲醇,該反應的熱化學方程式為:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗表面實驗室可用氨水洗滌銀鏡反應后的試管 | |
| B. | 實驗可以證明NH3結合Ag+能力比Cl-強 | |
| C. | 濁液中存在沉淀溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq) | |
| D. | 由資料信息科推知:加濃硝酸后生成的沉淀為AgCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可加入硫酸以提高電解質的導電性 | |
| B. | 放電時電池內部Li+向負極移動 | |
| C. | 充電過程中,電池正極材料的質量增加 | |
| D. | 放電時電池正極反應為:FePO4+Li++e-═LiFePO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| D | ||
| A | B | C |
| E |
| A. | 5Z | B. | 5Z+8 | C. | 5Z+10 | D. | 5Z+18 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com