
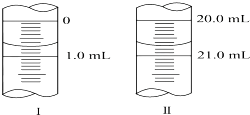
 在分析化學中常用Na2C2O4晶體作為基準物質測定KMnO4溶液的濃度.在H2SO4溶液中,反應如下:
在分析化學中常用Na2C2O4晶體作為基準物質測定KMnO4溶液的濃度.在H2SO4溶液中,反應如下:分析 (1)稱量固體時,無論開始時,還是稱量結束時,都需移動游碼,;使用天平時,移動游碼,應用鑷子撥動游碼;
(2)高錳酸鉀具有強氧化性,能腐蝕堿式滴定管的橡皮管;KMnO4溶液呈紫色,草酸反應完畢,滴入最后一滴KMnO4溶液,溶液由無色變為淺紫紅色,且半分鐘不褪色為滴定到終點;
(3)根據滴定管的結構、精確度以及測量原理來解答;根據關系式KMnO4~5Na2C2O4來計算;
(4)根據c(待測)=$\frac{V(標準)×c(標準)}{V(待測)}$分析不當操作對V(標準)的影響,以此判斷濃度的誤差.
解答 解:(1)若用托盤天平稱取W g Na2C2O4晶體,稱量開始時和稱量結束時的共同操作步驟是移動游碼,使游碼回零處,;稱量時需移動游碼,應用鑷子撥動游碼,
故答案為:把游碼撥回零處;鑷子;
(2)高錳酸鉀具有強氧化性,能腐蝕堿式滴定管的橡皮管,應裝在酸式滴定管中;KMnO4溶液呈紫色,草酸反應完畢,滴入最后一滴KMnO4溶液,溶液由無色變為淺紫紅色,且半分鐘不褪色為滴定到終點,
故答案為:酸式;滴入最后一滴KMnO4溶液,溶液由無色變為淺紫紅色,且半分鐘不褪色;
(3)滴定管的起始讀數為0.70mL,終點讀數為20.70mL,酸性KMnO4溶液消耗的體積為20.70mL-0.70mL=20.00mL;
KMnO4溶液的物質的量濃度為c,WgNa2C2O4配成100mL標準溶液,20.00mL溶液中含有Na2C2O4的質量為$\frac{w}{5}$g;
2KMnO4 ~5Na2C2O4
2moL 5×134g
0.02L×c $\frac{w}{5}$g
解得:c=$\frac{2w}{67}$mol•L-1,
故答案為:$\frac{2w}{67}$mol•L-1;
(4)溶液變色因局部過量而實際未達終點,立即讀數會造成V(標準)減小,根據c(待測)=$\frac{V(標準)×c(標準)}{V(待測)}$可知,所測結果偏低,
故答案為:偏低.
點評 本題主要考查了氧化還原反應滴定,涉及指示劑的原理、化學計算以及誤差分析,考查了學生分析問題和解決問題的能力.


科目:高中化學 來源: 題型:選擇題
| A. | 12g石墨和C60的混合固體中,含NA個碳原子 | |
| B. | 標準狀況下,2.24L水中含有0.1NA個水分子 | |
| C. | 7.8g過氧化鈉含有的共用電子對數為0.2NA | |
| D. | 5.6g鐵在足量氯氣中燃燒,電子轉移數目為0.2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放出堿液的滴定管開始有氣泡,發出液體后氣泡消失 | |
| B. | 滴定管用蒸餾水洗滌后,直接注入標準酸液進行滴定 | |
| C. | 錐形瓶用蒸餾水洗滌后,直接加入待測溶液滴定 | |
| D. | 滴定管用蒸餾水洗滌后,直接注入待測液,取20.00 mL進行滴定 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
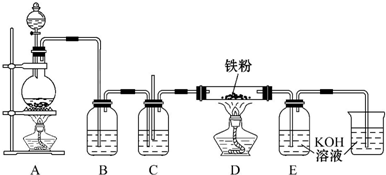
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
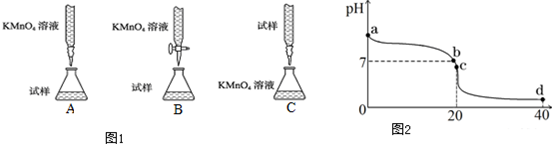
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 任何條件下,反應2CO2(g)═2CO(g)+O2(g)均不能自發進行 | |
| B. | 依據反應I2+2S2O32-═2I-+S4O62-,若要測定平衡體系I2+I-?I3-中平衡時的 c(I2),可用已知物質的量濃度的Na2S2O3溶液進行滴定實驗 | |
| C. | 向含有苯酚的苯溶液中滴入少量濃溴水未見白色沉淀,是因為生成的三溴苯酚又溶于苯中 | |
| D. | 檢驗某物質是否含有Fe2O3的操作步驟是:樣品粉碎→加水溶解→過濾,向濾液中滴加KSCN溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗目的 | 實驗操作 | |
| A | 配制1.0mol/L CuSO4溶液 | 把25g膽礬晶體溶于水配成100mL溶液 |
| B | 證明某溶液中含有SO42- | 向該溶液中滴入BaCl2溶液 |
| C | 實驗室制大量CO2 | 向稀硫酸中加入大理石 |
| D | 制備Fe(OH)3膠體 | 將飽和的FeCl3溶液滴加到熱NaOH溶液中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com