
分析 (1)向氨水中加入氯化鎂固體時,鎂離子和氫氧根離子反應生成氫氧化鎂沉淀,促進一水合氨電離;
(2)向氨水中加入濃鹽酸時,氫離子會消耗氫氧根離子,氫氧根離子濃度減小,促進一水合氨電離;
(3)向濃氨水中加入少量NaOH固體,導致溶液中氫氧根離子濃度增大,平衡向左移動.
解答 解:①向氨水中加入氯化鎂固體時,鎂離子和氫氧根離子反應生成氫氧化鎂沉淀,氫氧根離子濃度減小,促進一水合氨電離,則溶液中銨根離子濃度增大,
故答案為:右;減小;增大;
(2)向氨水中加入濃鹽酸時,氫離子會消耗氫氧根離子,氫氧根離子濃度減小,一水合氨的電離平衡向右移動,NH3、NH3•H2O的濃度均減小,
故答案為:右;OH-、NH3、NH3•H2O;
(3)向濃氨水中加入少量NaOH固體,導致溶液中氫氧根離子濃度增大,平衡向左移動,氫氧根離子和銨根離子反應生成氨氣,所以有刺激性氣體逸出,
故答案為:左;有刺激性氣體逸出.
點評 本題考查了弱電解質的電離,明確弱電解質電離特點是解本題關鍵,再結合溶液中離子濃度變化確定平衡移動方向,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | H+、Fe3+、SO42-、I- | B. | H+、NH4+、HCO3-、NO3- | ||
| C. | K+、AlO2-、Cl-、OH- | D. | Ag+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
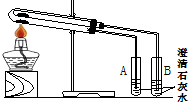 (1)為比較Na2CO3和NaHCO3的熱穩定性,某同學設計了如下實驗裝置.實驗時,先檢查裝置的氣密性,再取少量Na2CO3粉末加在大試管的底部,另取少量NaHCO3粉末加在小試管底部.預熱后在大試管底部加熱.
(1)為比較Na2CO3和NaHCO3的熱穩定性,某同學設計了如下實驗裝置.實驗時,先檢查裝置的氣密性,再取少量Na2CO3粉末加在大試管的底部,另取少量NaHCO3粉末加在小試管底部.預熱后在大試管底部加熱.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 被重結晶提純的物質的溶解度隨溫度變化大 | |
| B. | 溶解度很小的雜質留在了熱濾的濾渣里 | |
| C. | 重結晶的步驟為:加熱溶解、冷卻過濾、結晶 | |
| D. | 重結晶的首要工作是選擇適當的溶劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 乙醛的結構特點 | 可能的化學性質 |
| 有C=O雙鍵,不飽和 | 與H2發生加成反應,乙醛表現氧化性 |
CHO中C-H鍵極性較強 | CHO中C-H鍵被氧化,變為C-OH |
| 實驗 | 現象 | 結論 |
| 取適量乙醛溶液,滴加高錳酸鉀酸性溶液 | 高錳酸鉀溶液紫色變淺(褪去) | 乙醛能被高錳酸鉀氧化 |
| 向新制銀氨溶液中加入幾滴乙醛溶液,水浴加熱 | 試管壁上出現銀鏡(一層光亮如鏡的銀) | 乙醛將銀氨溶液還原 |
| 向新制氫氧化銅懸濁液中加入適量乙醛溶液,加熱 | 出現紅色沉淀 | 乙醛被氫氧化銅氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2A在水溶液中的電離方程式為H2A=2H++A2- | |
| B. | 該溫度下,將0.01mol/L的H2A溶液稀釋20倍后溶液的pH=3 | |
| C. | 體積相同,pH均為1的鹽酸和H2A溶液分別與足量的Zn反應,產生H2較多的是H2A | |
| D. | 將0.1mol/L的H2A溶液與0.2mol/L的氨水等體積混合后,溶液中濃度最大的離子是NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 14C與14N互為同位素 | B. | 淀粉和纖維素互為同分異構體 | ||
| C. | CH4與(CH3)2CHCH3互為同系物 | D. | H2O與D2O互為同素異形體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
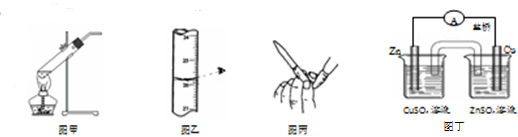
| A. | 用圖甲所示裝置加熱分解NaHCO3固體 | |
| B. | 用圖乙所示讀取滴定管讀數 | |
| C. | 用圖丙所示排堿式滴定管尖嘴內的氣泡 | |
| D. | 用圖丁所示裝置構成銅鋅原電池 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 已知:H2S在高溫下分解生成硫蒸氣和H2.現測得某溫度下,H2S分解過程中各物質的物質的量隨時間變化關系如圖所示,則生成的硫蒸氣化學式為( )
已知:H2S在高溫下分解生成硫蒸氣和H2.現測得某溫度下,H2S分解過程中各物質的物質的量隨時間變化關系如圖所示,則生成的硫蒸氣化學式為( )| A. | S | B. | S2 | C. | S6 | D. | S8 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com