
【題目】(2分)一定溫度下,可逆反應2NO2![]() 2NO+O2,在體積固定的密閉容器中反應,達到平衡狀態的標志是( )
2NO+O2,在體積固定的密閉容器中反應,達到平衡狀態的標志是( )
①單位時間內生成n mol O2,同時生成2n mol NO2;
②單位時間內生成n mol O2,同時生成2n mol NO;
③NO2、NO、O2的濃度比為2:2:1;
④混合氣體的壓強不再改變;
⑤混合氣體的顏色不再改變;
⑥混合氣體的平均摩爾質量不再改變.
A. ①④⑤⑥ B. ①②③⑤ C. ②③④⑥ D. 以上全部
【答案】A
【解析】在一定條件下,當可逆反應的正反應速率和逆反應速率相等時(但不為0),反應體系中各種物質的濃度或含量不再發生變化的狀態,稱為化學平衡狀態。則①單位時間內生成nmolO2是正反應,同時生成2nmolNO2是逆反應,且化學反應速率之比等于化學計量數之比,正逆反應速率相等,故①正確;②單位時間內生成nmolO2是正反應,同時生成2nmolNO也是正反應,故②錯誤;③任意時刻,化學反應速率之比都等于化學計量數之比,故用NO2與NO、O2表示的反應速率的比為2:2:1的狀態.不能作為判斷是否達到平衡狀態的依據,③錯誤;④反應前后氣體的體積不同,故混合氣體的壓強不再改變的狀態可作為判斷是否達到化學平衡狀態的依據,故④正確;⑤NO2為紅棕色氣體,O2和NO為無色氣體,故混合氣體的顏色不再改變,說明NO2濃度不變,可作為判斷是否達到化學平衡狀態的依據,故⑤正確;⑥平均分子量是氣體的總質量與總物質的量的比值,總質量不變,總物質的量在變,故混合氣體的平均相對分子質量不再改變的狀態可作為判斷是否達到化學平衡狀態的依據,⑥正確,故選A。


 小天才課時作業系列答案
小天才課時作業系列答案 一課四練系列答案
一課四練系列答案 黃岡小狀元滿分沖刺微測驗系列答案
黃岡小狀元滿分沖刺微測驗系列答案 新輔教導學系列答案
新輔教導學系列答案 陽光同學一線名師全優好卷系列答案
陽光同學一線名師全優好卷系列答案科目:高中化學 來源: 題型:
【題目】“結構決定性質,性質反映結構”是化學學科重要的學科思想,在有機化學中體現尤為明顯。據此回答下列問題:
(1)有機化學中把結構相似、分子組成相差若干個“CH2”原子團的有機化合物互稱為同 系物。同系物的化學性質一定_________(填“相同”、“相似”或“不同”),下列有機物中一定屬于同系物的是____________(填序號)。
①C3H4和C5H8 ②乙酸和硬脂酸(C17H35COOH)
③![]() 和
和![]() ④淀粉和纖維素 ⑤丙烯和聚乙烯
④淀粉和纖維素 ⑤丙烯和聚乙烯
⑥HOOCCH=CHCOOH和HOOCCH=C(CH3)COOH
(2)在有機物中,當同一官能團連接不同基團時,其表現出來的性質也有所不同。如有機物A(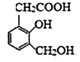 )的分子中有三種烴基(-OH),但由于其直接連接的基團不同而導致活潑性不同。下列轉化關系中選用的試劑為①________;②________;③_______。
)的分子中有三種烴基(-OH),但由于其直接連接的基團不同而導致活潑性不同。下列轉化關系中選用的試劑為①________;②________;③_______。

醛和酮的分子中都含有羰基(![]() ),但只有醛能被弱氧化劑氧化,請寫出葡萄糖與銀氨溶液反應的化學方程式:_____________ 。
),但只有醛能被弱氧化劑氧化,請寫出葡萄糖與銀氨溶液反應的化學方程式:_____________ 。
(3)某烴A,相對分子質量為140,其中碳的質量分數為0.857。A分子中有兩個碳原子 不與氫直接相連。A在一定條件下氧化只生成G,G能使石蕊試液變紅。
已知:
則產物G的結構簡式為__________ ,烴A在一定條件下生成高分子化合物的化學方程式為_______________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用98%濃硫酸配制500mL 2mol/L稀硫酸,下列操作使所配制濃度偏高的是
A. 量取濃硫酸時俯視量筒的刻度線
B. 定容時仰視500mL 容量瓶的刻度線
C. 量取硫酸后洗滌量筒并將洗滌液轉入容量瓶
D. 搖勻后滴加蒸餾水至容量瓶刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定濃度的CuSO4溶液與NaOH溶液反應會生成堿式鹽Cux(OH)y(SO4)z。為了測定該堿食鹽的
組成,進行了下列實驗:
①稱取樣品2.270g,用足量的稀鹽酸溶解配成50.00mL溶液,加入足量的BaCl2溶液,得到 BaSO4 l.l65g。
②另取樣品2.270g,溶于足量的稀硫酸配成l00.00mL溶液,取25.00mL溶液加入足量KI溶液 (化學方程式為2Cu2++4I-=2CuI↓+I2)充分反應后,以淀粉為指示劑,用0. 2500mol/LNa2S2O3溶液滴定生成的I2(離子方程式為2S2O32-+I2=2I-+S4O52-),消耗Na2S2O3溶液20.00mL。
(1)寫出CuSO4與NaOH反應生成Cux(OH)y(SO4)z的化學方程式______________(用x、y、z表示化學計量數)。
(2)滴定終點時溶液的顔色變化是__________。
(3)通過計算確定該堿食鹽的化學式(寫出計算過程)___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() I是常規核裂變產物之一,可以通過測定大氣或水中
I是常規核裂變產物之一,可以通過測定大氣或水中 ![]() I的含量變化來檢測核電站是否發生放射性物質泄漏.下列有關
I的含量變化來檢測核電站是否發生放射性物質泄漏.下列有關 ![]() I的敘述中錯誤的是( )
I的敘述中錯誤的是( )
A.![]() I的化學性質與
I的化學性質與 ![]() I相同
I相同
B.![]() I的質子數為53
I的質子數為53
C.![]() I的原子核外電子數為78
I的原子核外電子數為78
D.![]() I的原子核內中子數多于質子數
I的原子核內中子數多于質子數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,有可逆反應:2A(g)+2B(g) ![]() C(g)+3D(g);ΔH<0。現將2 mol A和2 mol B充入體積為V的甲容器,將2 mol C和6 mol D充入乙容器并使乙容器在反應開始前的體積為2V(如圖1)。
C(g)+3D(g);ΔH<0。現將2 mol A和2 mol B充入體積為V的甲容器,將2 mol C和6 mol D充入乙容器并使乙容器在反應開始前的體積為2V(如圖1)。

關于兩容器中反應的說法正確的是( )
A.兩容器達平衡后升高相同的溫度時,甲容器的反應速率大于乙容器的速率
B.兩容器中的反應均達平衡時,平衡混合物中各組份的體積百分組成相同,混合氣體的密度不同
C.甲容器中的反應先達到化學平衡狀態
D.在甲容器中再充入2mol A和2 mol B,平衡后甲中物質C的物質的量是乙中物質C的物質的量的2倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下的密閉容器中發生反應:2SO2(g) + O2(g)2SO3(g) ,若其他條件不變,下列措施會使該反應速率減小的是
A.升高溫度B.增大O2濃度C.加入催化劑D.減小壓強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】水泥是重要的建筑材料。水泥熟料的主要成分為CaO、SiO2,并含有一定量的鐵、鋁和鎂等金屬的氧化物。實驗室測定水泥樣品中鈣含量的過程如圖所示:

回答下列問題:
(1)在分解水泥樣品過程中,以鹽酸為溶劑,氯化銨為助溶劑,還需加入幾滴硝酸。加入H2O2的目的是__________。
(2)沉淀A不溶于強酸但可與一種弱酸反應,該反應的化學方程式為______________。
(3)沉淀B的主要成分為_________________________(填化學式)。
(4)草酸鈣沉淀經稀H2SO4處理后,用KMnO4標準溶液滴定,通過測定草酸的量可間接獲知鈣的含量,滴定反應為: ![]() +H++H2C2O4→Mn2++CO2+H2O。實驗中稱取0.400 g水泥樣品,滴定時消耗了0.0500 mol·L-1的KMnO4溶液36.00 mL,則該水泥樣品中鈣的質量分數為
+H++H2C2O4→Mn2++CO2+H2O。實驗中稱取0.400 g水泥樣品,滴定時消耗了0.0500 mol·L-1的KMnO4溶液36.00 mL,則該水泥樣品中鈣的質量分數為
______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求完成下列填空:
(1)畫出Mg原子結構示意圖: , O2﹣結構示意圖: .
(2)現有以下物質:①NaCl溶液;②Cu;③乙醇(C2H5OH);④熔融的KNO3;⑤BaSO4固體;⑥干冰.
其中:屬于電解質的是;屬于非電解質的是;能導電的是(以上都用序號填寫).
(3)11.0g 由 ![]() 和
和 ![]() 組成的水分子,其中含中子數為mol,電子數為mol.
組成的水分子,其中含中子數為mol,電子數為mol.
(4)已知某植物營養液配方為0.3mol KCl,0.2mol K2SO4 , 0.1mol ZnSO4和1L水.若以KCl,K2SO4 , ZnCl2和1L水為原料配得相同組成的營養液,需三種溶質KClmol,K2SO4mol,ZnCl2mol.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com