
分析 (1)計算NO物質的量,再計算NO2、N2O4總物質的量,氣體全部為NO、NO2時,得到硝酸最少,氣體為NO、N2O4時得到硝酸最多,結合N原子守恒計算;
(2)根據c=$\frac{1000ρω}{M}$計算98%濃硫酸密度、87%硫酸的物質的量濃度,再根據稀釋定律計算吸水后硫酸體積,進而吸收水的質量;
(3)根據蒸餾過程中硝酸、硝酸鎂質量不變,表示出蒸餾后97.5%的HNO3的質量、60%的Mg(NO3)2溶液質量,蒸餾后溶液質量之和=原溶液質量之和-損耗水的質量;
(4)根據N原子守恒計算n(NaNO3),NO、NO2和NaOH溶液反應方程式為:2NO2+2NaOH=NaNO2+NaNO3+H2O和NO+NO2+2NaOH=2NaNO2+H2O,結合方程式計算原混合氣體中NO和NO2的物質的量,再根據氧原子守恒解答.
解答 解:(1)NO的物質的量為1.25mol×0.6=0.75mol,則NO2、N2O4總物質的量為1.25mol-0.75mol=0.5mol,
氣體全部為NO、NO2時,得到硝酸最少,根據N原子守恒,得到硝酸極小值為1.25mol,
氣體為NO、N2O4時得到硝酸最多,根據N原子守恒,得到硝酸極大值為0.75mol+0.5mol×2=1.75mol,
則:1.25mol<n(HNO3)<1.75mol,
故答案為:1.25mol<n(HNO3)<1.75mol;
(2)98%濃硫酸密度為$\frac{18.4×98}{1000×98%}$g/mL=1.84g/mL,
87%(密度1.8g/cm3)的硫酸物質的量濃度為$\frac{1000×1.8×87%}{98}$mol/L,
根據稀釋定律,50mL濃硫酸吸水失去吸水能力后溶液體積為:$\frac{50mL×18.4mol/L}{\frac{1000×1.8×87%}{98}mol/L}$=57.57mL,
則吸收水的質量為:$\frac{50mL×18.4mol/L}{\frac{1000×1.8×87%}{98}mol/L}$×1.8g/mL-50mL×1.84g/mL=11.63g
故答案為:11.63;
(3)蒸餾后得到97.5%的HNO3的質量為$\frac{{m}_{1}×65%}{97.5%}$,得到60%的Mg(NO3)2溶液質量為$\frac{{m}_{2}×72%}{60%}$,損耗水的總質量為(m1+m2)×5%,則:
$\frac{{m}_{1}×65%}{97.5%}$+$\frac{{m}_{2}×72%}{60%}$=(m1+m2)-(m1+m2)×5%
整理可得:$\frac{{m}_{1}}{{m}_{2}}$=0.88
故答案為:0.88;
(4)根據N原子守恒得n(NaNO3)=n(NOx)-n(NaNO2)=0.5mol-0.35mol=0.15mol,
由 2NO2+2NaOH=NaNO2+NaNO3+H2O,可知生成0.15mol硝酸鈉需要0.3molNO2,同時生成0.15mol亞硝酸鈉,則反應NO+NO2+2NaOH=2NaNO2+H2O生成的亞硝酸鈉為0.35mol-0.15mol=0.2mol,則該反應中消耗0.1molNO2、0.1molNO,所以原混合氣體中NO、NO2的物質的量分別是0.1mol、0.4mol,尾氣中NO與NO2的平均組成記為NOx,則x=$\frac{0.1mol×1+0.4mol×2}{0.5mol}$=1.8,
故答案為:1.8.
點評 本題考查混合物有關計算、溶液濃度計算,題目計算量大,屬于易錯題目,有利于培養學生的分析計算能力,注意極限法與守恒法的應用,難度中等.


科目:高中化學 來源: 題型:多選題
| A. | KOH | B. | Na2CO3 | C. | HClO4 | D. | MgSO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 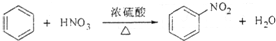 | |
| B. |  | |
| C. | CH3CH2OH+CH3COOH$?_{△}^{濃硫酸}$CH3COOCH2CH3+H2O | |
| D. | CH4+Cl2$\stackrel{光照}{?}$CH3Cl+HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氣體的平均分子量不再變化 | B. | 反應的平衡常數不變 | ||
| C. | ?(H2)=2 ?(HI) | D. | 氣體的顏色不再變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:6 | B. | 2:15 | C. | 2:3 | D. | 16:25 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
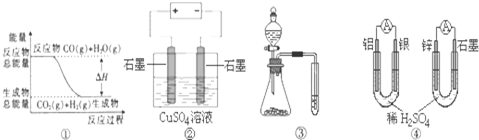
| A. | 圖①表示可逆反應“CO(g)+H2O(g)?CO2(g)+H2(g)”中的△H大于0 | |
| B. | 圖②為電解硫酸銅溶液的裝置,一定時間內,兩電極產生單質的物質的量之比一定為1:1 | |
| C. | 圖③實驗裝置可完成比較磷酸、碳酸、苯酚的酸性強弱的實驗 | |
| D. | 圖④兩個裝置中通過導線的電子數相同時,消耗負極材料的物質的量也相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用磨口玻璃瓶、玻璃塞保存NaOH溶液 | |
| B. | 加入適量的金屬鈉除去酒精中少量的水 | |
| C. | 分液時,分液漏斗中的上層液體應由上口倒出 | |
| D. | 能使濕潤的淀粉碘化鉀試紙變藍色的氣體一定是Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
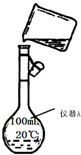 化學是一門以實驗為基礎的學科,化學所取得的豐碩成果,是與實驗的重要作用分不開的.結合右側下列實驗裝置圖回答有關問題:
化學是一門以實驗為基礎的學科,化學所取得的豐碩成果,是與實驗的重要作用分不開的.結合右側下列實驗裝置圖回答有關問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com