
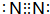 .
.分析 X的水溶液的pH<7,則X為強酸弱堿鹽,在一定條件下,SCl2與氨完全反應生成A和淡黃色單質B及離子化合物X,根據元素守恒知淡黃色單質B為S、X為NH4Cl,某無機化合物A的相對分子質量為184,18.4gA的物質的量=$\frac{18.4g}{184g/mol}$=0.1mol,根據質量守恒定律得C質量為18.4g-12.8g=5.6g,A分解生成S和單質C,則A是二元化合物且含有S元素,SCl2與氨反應生成NH4Cl,氨氣中N、H原子個數比為1:3、氯化銨中N、H原子個數比為1:4,根據原子守恒知,A中還含有N元素,所以C為N2,n(S)=$\frac{12.8g}{32g/mol}$=0.4mol、n(S)=$\frac{5.6g}{14g/mol}$=0.4mol,所以A中N、S原子個數之比為0.4mol:0.4mol=1:1,所以A為S4N4,
據此分析解答.
解答 解:(1)通過以上分析知,A的化學式為S4N4,C是氮氣,其電子式為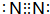 ,故答案為:S4N4;
,故答案為:S4N4;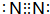 ;
;
(2)一定條件下,SCl2與氨反應生成S、氯化銨和S4N4,反應方程式為6SCl2+16NH3$\frac{\underline{\;一定條件下\;}}{\;}$S4N4+2S+12NH4Cl,
故答案為:6SCl2+16NH3$\frac{\underline{\;一定條件下\;}}{\;}$S4N4+2S+12NH4Cl;
(3)亞硝酸鈉中N元素化合價為+3價、氯化銨中N元素化合價為-3價,二者可以發生氧化還原反應生成0價的氮氣,故答案為:可能;NaNO2中N元素化合價為+3價,NH4Cl中N元素化合價為-3價,發生氧化還原反應生成N2;
(4)X為氯化銨,氯離子可以用硝酸酸化的硝酸銀檢驗,銨根離子可以用NaOH、濕潤的紅色石蕊試紙檢驗,其檢驗方法是:取少量X固體加水溶解,分成兩份;其中一份加入濃NaOH溶液加熱,若產生能使濕潤的紅色石蕊試紙變藍的氣體,則證明有NH4+;向另一份溶液中加入硝酸酸化的AgNO3溶液,若出現白色沉淀,則證明有Cl-,
故答案為:取少量X固體加水溶解,分成兩份;其中一份加入濃NaOH溶液加熱,若產生能使濕潤的紅色石蕊試紙變藍的氣體,則證明有NH4+;向另一份溶液中加入硝酸酸化的AgNO3溶液,若出現白色沉淀,則證明有Cl-.
點評 本題考查無機物推斷,涉及S、N元素及其化合物之間的轉化,根據氨氣與SCl2反應前后N、H元素原子個數比確定A是解本題關鍵,熟悉常見離子的檢驗方法,易錯點是化學用語的靈活運用,題目難度中等.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 聚丙烯的結構簡式: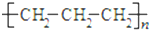 | |
| B. | 乙炔的分子結構模型示意圖: | |
| C. | H2O2的電子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| D. |  的名稱:3-甲基-1-丁醇 的名稱:3-甲基-1-丁醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
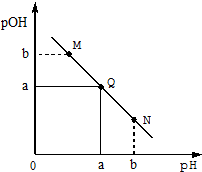 某溫度下,向一定體積0.1mol/LHCl溶液中逐滴加入等濃度的氨水溶液,溶液中pOH[pOH=-lgc(OH-)]與pH的變化關系如右圖所示,則下列
某溫度下,向一定體積0.1mol/LHCl溶液中逐滴加入等濃度的氨水溶液,溶液中pOH[pOH=-lgc(OH-)]與pH的變化關系如右圖所示,則下列| A. | Q點消耗氨水溶液的體積等于HCl溶液的體積 | |
| B. | M點所示溶液導電能力弱于Q點 | |
| C. | M點和N點所示溶液中水的電離程度相同 | |
| D. | N點所示溶液中c(NH4+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
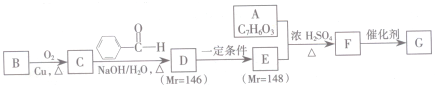

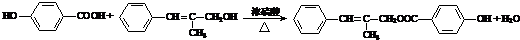 .
. .
. (其中任一種).
(其中任一種).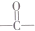 結構②苯環上有2個取代基.
結構②苯環上有2個取代基.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 0.1 mol•L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 0.1 mol•L-1NaHCO3溶液與0.1 mol•L-1NaOH溶液等體積混合:c(Na+)=2c(CO32-)+c(HCO3-)+2c(H2CO3) | |
| C. | 0.1 mol•L-1NaHCO3溶液與0.2 mol•L-1NaOH溶液等體積混合:c(Na+)>c(OH-)>0.05 mol•L-1>c(CO32-)>c(HCO3-) | |
| D. | 0.2 mol•L-1NaHCO3溶液與0.1 mol•L-1NaOH溶液等體積混合:c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 重金屬離子Ag+、Cu2+、K+均可導致蛋白質變性 | |
| B. | S02和NxOy都屬于非金屬氧化物,也都是酸性氧化物 | |
| C. | 部分顆粒分散在空氣中可能會形成丁達爾現象 | |
| D. | 苯和苯的衍生物都是芳香烴 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 某同學設計了如圖所示的套管實驗裝置(部分裝置未畫出)來制備SO2并利用實驗現象來檢驗其還原性,制備SO2時選用的試劑為Cu和濃H2SO4.回答下列問題:
某同學設計了如圖所示的套管實驗裝置(部分裝置未畫出)來制備SO2并利用實驗現象來檢驗其還原性,制備SO2時選用的試劑為Cu和濃H2SO4.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com