
 某同學設計了如圖所示的套管實驗裝置(部分裝置未畫出)來制備SO2并利用實驗現象來檢驗其還原性,制備SO2時選用的試劑為Cu和濃H2SO4.回答下列問題:
某同學設計了如圖所示的套管實驗裝置(部分裝置未畫出)來制備SO2并利用實驗現象來檢驗其還原性,制備SO2時選用的試劑為Cu和濃H2SO4.回答下列問題:分析 (1)Cu與濃硫酸在加熱條件下反應生成硫酸銅、二氧化硫與水;
(2)反應中硫酸中S元素部分化合價降低生成二氧化硫,部分未變化生成硫酸銅;
(3)利用實驗現象檢驗SO2的還原性,應選擇含有具有強氧化性的試劑,且反應現象明顯.
解答 解:(1)Cu與濃硫酸在加熱條件下反應生成硫酸銅、二氧化硫與水,反應方程式為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O,
故答案為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O;
(2)反應中硫酸中S元素部分化合價降低生成二氧化硫,部分未變化生成硫酸銅,反應中硫酸表現:氧化性、酸性,
故答案為:氧化性、酸性;
(3)利用實驗現象檢驗SO2的還原性,雙氧水、酸性高錳酸鉀溶液具有強氧化性,二氧化硫與雙氧水反應沒有明顯現象,故選擇酸性高錳酸鉀溶液,現象是:酸性高錳酸鉀溶液褪色,
故答案為:C; 酸性高錳酸鉀溶液褪色.
點評 本題考查濃二氧化硫的制備及性質實驗,難度不大,側重考查學生對知識的遷移應用,有利于基礎知識的鞏固.


 寒假學與練系列答案
寒假學與練系列答案科目:高中化學 來源: 題型:解答題
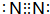 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
時間(min) 濃度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
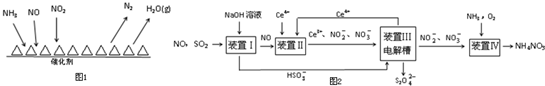
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH相等的①NH4Cl②(NH4)2SO4③NH4HSO4溶液:c(NH4+)大小順序為①>②>③ | |
| B. | 0.2mol•L-1CH3COOH溶液和0.2mol•L-1CH3COONa溶液等體積混合:c(CH3COOH)+c(CH3COO-)=2c(Na+) | |
| C. | 0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 0.1mol•L-1NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
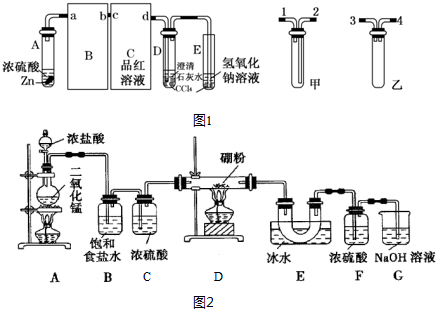
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
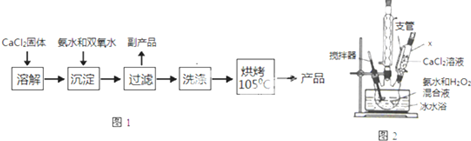
| 實驗序號 | 第1次 | 第2次 | 第3次 | 第4次 |
| 消耗KMnO4體積/mL | 19.98 | 20.02 | 20.20 | 20.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 所有主族元素的最高正化合價都等于其最外層電子數 | |
| B. | 所有過渡元素都是金屬元素,所有的金屬元素也都是過渡元素 | |
| C. | 在周期表中氧族元素的單質全部是氣體 | |
| D. | 同周期主族元素的原子半徑以ⅦA族的為最小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com