
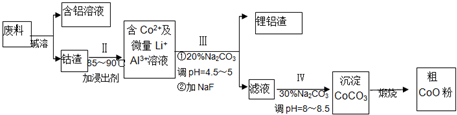
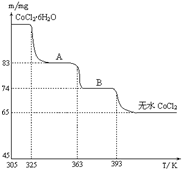
| 238 |
| m |
| 130 |
| 65mg |
| 238 |
| 119mg |
| 18(6-n) |
| 119mg-74mg |


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
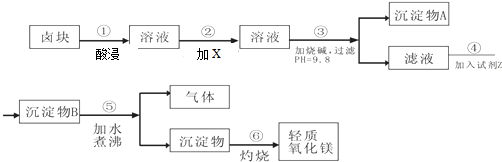
| 物質 | 開始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| 試劑 | 價格(元/噸) |
| 漂液(含NaClO,25.2%) | 450 |
| 雙氧水(含H2O2,30%) | 2400 |
| 燒堿(含98% NaOH) | 2100 |
| 純堿(含99.5% Na2CO3) | 600 |
查看答案和解析>>
科目:高中化學 來源: 題型:
2- 3 |
2- 4 |
2- 3 |
2- 4 |
2- 3 |
2- 4 |
2- 3 |
2- 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
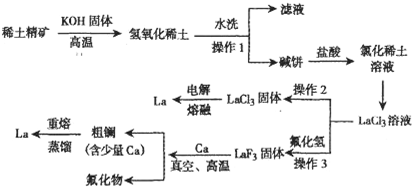
| 金屬 | 熔點(℃) | 沸點(℃) |
| 鈣 | 841 | 1487 |
| 鑭 | 920 | 3470 |
查看答案和解析>>
科目:高中化學 來源: 題型:
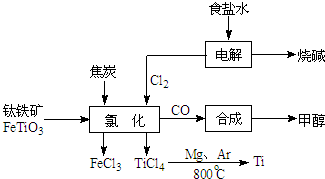
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
| 試管 | 未加MnSO4的試管 | 加有MnSO4的試管 |
| 褪色時間 | 30s | 2s |
| 試管 | 未滴加稀硫酸的試管 | 滴加了稀硫酸的試管 |
| 褪色時間 | 100s | 90s |
| 試管 | 滴入10滴稀硫酸的試管 | 加入1mL稀硫酸的試管 | 加入2mL稀硫酸的試管 |
| 褪色時間 | 70s | 100s | 120s |
| Mn2+ |
| Mn2+ |
| Mn2+ |
| C2O42- |
查看答案和解析>>
科目:高中化學 來源: 題型:
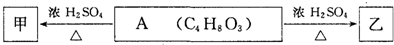
| HCl |
| △ |
| HCl |
| △ |
| NH3 |
| △ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com