
| A. | ①③⑤ | B. | ②③⑤ | C. | ②③④ | D. | ②③④⑤ |
分析 比較非金屬元素的非金屬性強弱,可根據單質之間的置換反應、對應最高價氧化物的水化物的酸性、氫化物的穩定性等化學性質的角度判斷,Cl的非金屬性比S的非金屬性強弱與物理性質無關.
解答 解:①常溫時硫是固體,而氯氣為氣體,都是物理性質,與非金屬性無關,所以無法說明非金屬性的強弱,故錯誤;
②元素的非金屬性越強,其單質與氫氣化合越容易,Cl2與H2混合,強光照射劇烈反應,而S與H2反應需較高溫度,氯氣比S與氫氣反應容易,則說明非金屬性Cl>S,故正確;
③非金屬單質與金屬單質反應,生成產物的化合價越高,則非金屬單質的氧化性越強,所以Cl2的氧化性大于S的氧化性,所以Cl的非金屬性比S的強,故正確;
④比較元素的非金屬性應用元素對應最高價氧化物的水化物的酸性強弱比較,不能根據氫化物的酸性強弱比較,例如鹽酸的酸性比氫硫酸強,非金屬性:Cl>S,但HF溶液的酸性比HCl弱,但非金屬性:F>Cl,不能說明非金屬性的強弱,故錯誤;
⑤將Cl2通入氫硫酸中可置換出S,說明氯氣的氧化性比S強,單質的氧化性越強,非金屬性越強,所以能證明Cl的非金屬性比S的強,故正確;
則正確的有②③⑤;
故選B.
點評 本題考查非金屬性的比較角度,題目難度不大,注意把握比較非金屬性的方法,非金屬性屬于化學性質,與物理性質無關,非金屬性強弱與失電子多少無關,題目難度不大.


 金鑰匙試卷系列答案
金鑰匙試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | Al、Mg、Na | B. | Mg、Al、Na | C. | Na、Mg、Al | D. | Na、Al、Mg |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 平衡混合氣的平均相對分子質量 | |
| B. | 平衡混合氣中一種反應物的濃度 | |
| C. | 平衡混合氣中一種生成物的體積分數 | |
| D. | 平衡混合氣中一種反應物的體積分數 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,11.2L苯中含有C-H鍵的數目為3NA | |
| B. | 常溫下,1.0LPH=13的Ba(OH)2溶液中含有的OH-數目為0.1NA | |
| C. | 常溫下,56g鐵片投入足量濃H2SO4中生成NA個SO2分子 | |
| D. | 電解飽和食鹽水,陽極產生22.4L氣體時,電路中通過的電子數目為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
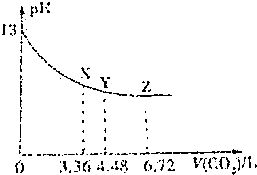
| A. | 該NaOH溶液的濃度為0.1mol/L,體積為6L | |
| B. | X、Y、Z三點對應的溶液中離子的種類不同 | |
| C. | Y點對應的融資中離子濃度關系為:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| D. | Y點對應的溶液中存在著:c(Na+)=2c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(Mg2+)>c(Mn2+) | |
| B. | c(Mg2+)=c(Mn2+) | |
| C. | c(Mg2+)<c(Mn2+) | |
| D. | 沉淀類型不同,無法用Ksp比較二種離子的濃度 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com