
| T/K | 298 | 398 | 498 |
| 平衡常數K | 4.1×106 | K1 | K2 |
分析 (1)①根據升高溫度平衡吸熱方向移動以及平衡逆向移動平衡常數減小;
②直接標志:①速率關系:正反應速率與逆反應速率相等,②反應體系中各物質的百分含量保持不變.
間接標志:①混合氣體的總壓強、總體積、總物質的量不隨時間的改變而改變(m+n≠p+q);②各物質的濃度、物質的量不隨時間的改變而改變;③各氣體的體積、各氣體的分壓不隨時間的改變而改變;
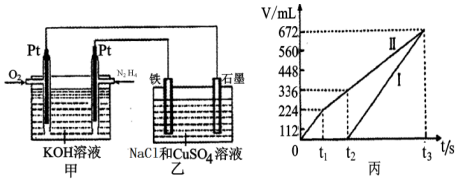
(2)電池通入肼N2H4的為負極,乙中石墨電極為陽極、鐵電極為陰極,開始Cl-在陽極放電生成氯氣,陰極Cu2+放電生成Cu,故圖丙中Ⅰ表示陰極產生的氣體,Ⅱ表示陽極產生的氣體,t1前電極反應式為:陽極2Cl--4e-=Cl2↑,依據生成的遷移體積計算物質的量得到氯化鈉物質的量計算濃度,陰極2Cu2++4e-=2Cu,t1~t2電極反應式為:陽極4OH--4e-=O2↑+2H2O,陰極2Cu2++4e-=2Cu,t2點后電極反應式為:陽極4OH--4e-=O2↑+2H2O,陰極4H++4e-=2H2↑,所以t1~t2 陽極上生成氧氣,根據氧氣的量計算氫氧根離子的物質的量,水電離出等物質的量的氫離子和氫氧根離子,根據公式計算得出C(H+),從而得出溶液的pH.
解答 解:(1)①N2(g)+3H2(g)?2NH3(g)△H<0為放熱反應,升高溫度,平衡逆向移動,平衡常數減小,所以K2<K1,
故答案為:<;
③a.平衡時反應混合物中各組分的含量保持不變,但容器內N2、H2、NH3的濃度之比不一定為為1:3:2,所以不能作為平衡的標志,故a錯誤;
b.平衡時不同物質表示速率之比等于系數之比說明到達平衡,即3v(N2)正=v(H2)逆說明反應達到平衡,故b錯誤;
c.反應前后氣體體積減小,若壓強不變,說明反應達到平衡,故c正確;
d.反應前后氣體的質量不變,容器的體積不變,所以密度不變,所以混合氣體的密度保持不變不能作為平衡的標志,故d錯誤;
故答案為:c;
(2)①肼燃料電池中,在堿性條件下,N2H4失電子生成氮氣與水,電極反應式為:N2H4+4OH--4e-=N2↑+4H2O,
故答案為:N2H4+4OH--4e-=N2↑+4H2O;
②乙中石墨電極為陽極、鐵電極為陰極,開始Cl-在陽極放電生成氯氣,陰極Cu2+放電生成Cu,故圖丙中Ⅰ表示陰極產生的氣體,Ⅱ表示陽極產生的氣體,t1前電極反應式為:陽極2Cl--4e-=Cl2↑,生成氯氣為224mL,由2Cl--2e-=Cl2↑可知,n(NaCl)=2n(Cl2)=$\frac{0.224L}{22.4L/mol}$×2=0.02mol,所以c(NaCl)=$\frac{0.02mol}{0.1L}$=0.2mol/L;
故答案為:0.2mol/L;
③t2點后電極反應式為:陽極4OH--4e-=O2↑+2H2O,陰極4H++4e-=2H2↑,所以t1~t2 陽極上生成氧氣,t1~t2Ⅱ產生的氣體體積=0.336L-0.224L=0.112L,陽極上生成112mL氧氣需要n(OH-)=$\frac{0.112L×4}{22.4L/mol}$=0.02mol,水電離出等物質的量的氫離子和氫氧根離子,所以n(H+)=0.02mol,c(H+)=$\frac{0.02mol}{0.1L}$=0.2mol/L,所以溶液的pH=1-lg2=0.7,
故答案為:0.7.
點評 本題考查較為綜合,涉及化學平衡的有關計算、電解池原理等知識點,題目難度中等,注意電解硫酸銅和氯化鈉混合溶液時,明確離子的放電順序是解本題的關鍵,試題培養了學生的分析能力及靈活應用能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2F2+2H2O=4HF+O2反應中,水作還原劑,失電子 | |
| B. | 2Na+2H2O=2NaOH+H2↑反應中,水被氧化 | |
| C. | CH4+2O2$\frac{\underline{\;點燃\;}}{\;}$ CO2+2H2O反應中,H2O是還原產物 | |
| D. | Na2O+H2O=2Na++2OH-反應中,水既不是氧化劑也不是還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
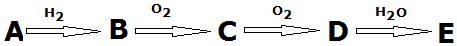
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | MnO4-、SO42-、I-、Na+ | B. | Na+、Cu2+、S2-、NO3- | ||
| C. | K+、Al3+、HCO3-、SO42- | D. | Na+、K+、Cl-、ClO- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 摩爾既是物質的數量單位又是物質的質量單位 | |
| B. | 阿伏加德羅常數是 12kg12C中含有的碳原子數 | |
| C. | 1molH2O中含有2mol H和1mol O | |
| D. | 一個NO分子的質量是ag,一個NO2分子的質量是bg,則氧原子的摩爾質量是(b-a)g/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | K+、Cu2+、OH-、SO42- | B. | K+、Na+、Cl-、NO3- | ||
| C. | Zn2+、NH4+、NO3+、Cl- | D. | K+、Na+、CO32-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
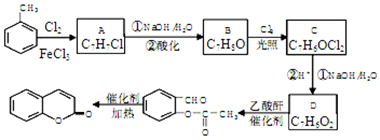
 ,A→B的反應類型是取代反應.
,A→B的反應類型是取代反應.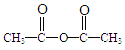 )反應,除生成
)反應,除生成 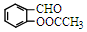 外,同時生成的另一種產物的結構簡式是CH3COOH.
外,同時生成的另一種產物的結構簡式是CH3COOH.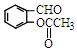 互為同分異構體,且具有以下特點:
互為同分異構體,且具有以下特點:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在KClO3+6HCl=3Cl2↑+KCl+3H2O中,被氧化的氯原子和被還原的氯原子的個數比為6:1 | |
| B. | 在反應:2KNO3+3C+S=K2S+N2↑+3CO2↑,則被還原的元素為氮和硫 | |
| C. | 失電子能力難的原子獲得電子的能力一定強 | |
| D. | 在化學反應中某元素由化合態變為游離態,該元素一定被還原了 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com