
| 電負性 | 鍵長 | 鍵的極性 | 沸點(同壓) |
| C<N | C=C<C-C | N-H<O-H | 甲醇>丁烷 |
分析 (1)C的原子序數為6,原子結構中有2個電子層,最外層電子數為4;Cr的原子核外有24個電子,分4層排布;根據乙炔的結構分析;
(2)同周期從左到右電負性增強;
鍵長越短,鍵能越大;
非金屬性越強,鍵的極性越強;
分子間含有氫鍵時沸點較高;
(3)已知①2Na(s)+$\frac{1}{2}$O2(g)=Na2O(s)△H=-414kJ•mol-1
②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ•mol-1
由蓋斯定律:2×①-②得Na(s)+Na2O2(s)=2Na2O(s)據此計算;
(4)乙醇與CrO3和少量H2SO4反應生成硫酸鉻、二氧化碳和水.
解答 解:(1)C的原子序數為6,原子結構中有2個電子層,最外層電子數為4,C元素位于元素周期表第二周期,第IVA族;Cr的原子核外有24個電子,分4層排布,其電子排布式為:1s22s22p63s23p63d54s1;乙炔的結構為H-C≡C-H,單鍵中含有1個σ鍵,三鍵中含有1個σ鍵和2個π鍵,則分子中σ鍵與π鍵數目之比為 3:2;
故答案為:二;IVA;1s22s22p63s23p63d54s1;3:2;
(2)同周期從左到右電負性增強,則電負性:C<N;
鍵長越短,鍵能越大,雙鍵的鍵能大于單鍵,則雙鍵的鍵長小于單鍵;
非金屬性O>S,則鍵的極性:N-H<O-H;
分子間含有氫鍵時沸點較高,甲醇分子間含有氫鍵,則沸點:甲醇>丁烷,
故答案為:<;<;<;>;
(3)已知①2Na(s)+$\frac{1}{2}$O2(g)=Na2O(s)△H=-414kJ•mol-1
②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ•mol-1
由蓋斯定律:2×①-②得Na(s)+Na2O2(s)=2Na2O(s)△H=2×(-414)-(-511)=-317 kJ•mol-1;
故答案為:Na(s)+Na2O2(s)=2Na2O(s)△H=-317 kJ•mol-1;
(4)乙醇與CrO3和少量H2SO4反應生成硫酸鉻、二氧化碳和水,其反應的化學方程式為:C2H5OH+4CrO3+6H2SO4=2Cr2(SO4)3+2CO2↑+9H2O;
故答案為:C2H5OH+4CrO3+6H2SO4=2Cr2(SO4)3+2CO2↑+9H2O.
點評 本題考查較綜合,涉及電子排布式、元素周期表的結構及應用、元素非金屬性的比較及應用、氫鍵、蓋斯定律的應用等,注重高頻考點的考查,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
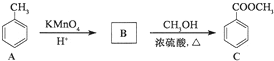
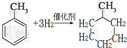 ,反應類型為加成反應.
,反應類型為加成反應.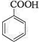 ,所得B的粗產品通常用重結晶的方法提純.
,所得B的粗產品通常用重結晶的方法提純.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
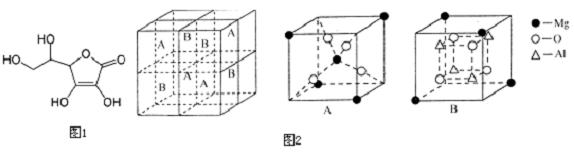
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ,E、H中所含官能團的名稱分別是羥基、碳碳雙鍵.
,E、H中所含官能團的名稱分別是羥基、碳碳雙鍵. +CH3CH2OH$→_{△}^{濃硫酸}$
+CH3CH2OH$→_{△}^{濃硫酸}$ +H2O、n
+H2O、n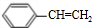 $\stackrel{催化劑}{→}$
$\stackrel{催化劑}{→}$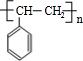 .
. (寫出其中一種的結構簡式).
(寫出其中一種的結構簡式).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②⑤ | C. | ②③⑤ | D. | ②③④⑤⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 72 | B. | 53 | C. | 19 | D. | 125 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
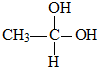 →CH3-CHO+H2O
→CH3-CHO+H2O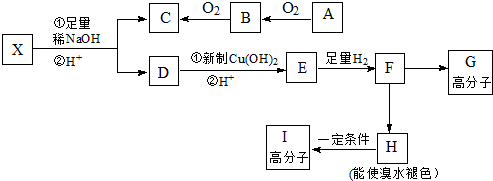
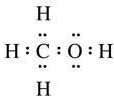 .
. ;
;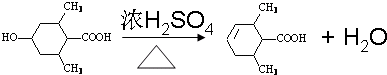 ;
;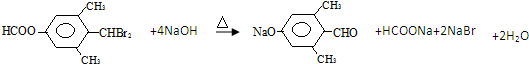 ;
;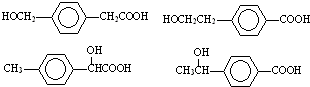 任意一種.
任意一種.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe2+、Mg2+、SO42-、NO3- | B. | Na+、Ag+、Br-、PO43- | ||
| C. | Ba2+、K+、SO32-、ClO- | D. | Al3+、NH4+、CO32-、Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com