
【題目】甲、乙、丙是三種常見的單質,A、B、C是三種常見的二元無機化合物,它們之間的轉化關系如右圖所示。請回答下列有關問題:
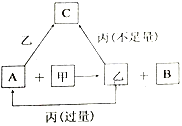
(1)若甲為常見氣態非金屬單質,丙為金屬單質,三種單質中只有甲由短周期元素組成;甲與乙同主族、乙與丙同周期;它們的轉化關系均在溶液中進行。則:
①甲物質的名稱為___________。
②丙元素在元素周期表中的位置是___________。
③反應A+甲→乙+B的離子方程式為______________________。
④請簡述B中陽離子的檢驗方法__________________________________。
(2)若甲為常見金屬單質,乙為常見固態非金屬單質,且所有物質組成元素均為短周期元素。則:
①乙的化學式為___________。
②A的電子式為___________。
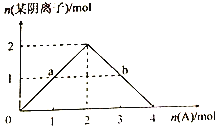
③將A緩慢通入氫氧化鈉溶液中,所得溶液中的某種陰離子的物質的量隨n(A)的通入轉化關系如右圖所示。圖中a、b兩點的溶液中水的電離程度的大小關系為a_______b(填“>”、“=”或“<")。若溶液X為圖中曲線上任意一點,則向溶液X中逐滴加入鹽酸至反應完全,消耗鹽酸的物質的量最大為___________。
【答案】 氯氣 第四周期第Ⅷ族 2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- 用試管取少量B溶液,然后向其中滴入幾滴KSCN溶液,若溶液呈現血紅色,證明有Fe3+存在 C ![]() < 4mol
< 4mol
【解析】根據題給信息,A+甲→乙+B 該反應為置換反應,若甲為常見氣態非金屬單質,三種單質中只有甲由短周期元素組成,甲與乙同主族;根據周期表中主族元素的置換規律:氯氣置換溴,所以甲為氯,乙為溴,乙與丙同周期,丙為鐵,A為溴化亞鐵,B為氯化鐵,溴與過量的鐵生成溴化亞鐵,溴與少量的鐵生成溴化鐵;
①正確答案:氯氣;
② 鐵元素在周期表中第四周期,第Ⅷ族;正確答案:第四周期、第Ⅷ族;
③ 溴化亞鐵被氯氣全部氧化為單質溴和氯化鐵,該反應為置換反應;正確答案:
2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-;
④Fe3+的最簡的檢驗方法滴加KSCN溶液,若溶液變為血紅色,溶液中含有Fe3+;正確答案:用試管取少量B溶液,然后向其中滴入幾滴KSCN溶液,若溶液呈現血紅色,證明有Fe3+存在;
(2)甲為常見金屬單質,乙為常見固態非金屬單質,且所有物質組成元素均為短周期元素;
A+甲→乙+B 該反應為置換反應,金屬置換非金屬反應,金屬鎂在二氧化碳氣體中燃燒,生成碳單質和氧化鎂;A為二氧化碳,甲為鎂,乙為碳,B為氧化鎂;碳與足量的氧氣燃燒變為二氧化碳,氧氣不足,生成一氧化碳;
① 正確答案:C;
② 正確答案:![]()
③將二氧化碳緩慢通入氫氧化鈉溶液中,當達到a點時,生成部分碳酸鈉,所得混合液為氫氧化鈉和碳酸鈉;當二氧化碳繼續通入,氫氧化鈉完全反應,正好生成碳酸鈉溶液,曲線達到最高點;繼續通入二氧化碳,碳酸鈉繼續與二氧化碳反應,達到b 點,溶液變為碳酸鈉和碳酸氫鈉的混合液,直到最后,碳酸鈉全部變為碳酸氫鈉溶液; a點為氫氧化鈉和碳酸鈉混合液,溶液為強堿,抑制水的電離;b 點碳酸鈉和碳酸氫鈉的混合液,兩種鹽都能夠促進水的電離,a<b; 正確答案:< ;從圖像上看,當反應進行到最大值時,,陰離子的總量為2mol,恰好生成碳酸鈉溶液,n(Na+)=4 mol, 向溶液X中逐滴加入鹽酸至反應完全,,所得溶液的溶質為氯化鈉,根據守恒原則,n(Cl-)=n(HCl)=4 mol,正確答案:4 mol;
.


科目:高中化學 來源: 題型:
【題目】在一塊表面無銹的鐵片上滴食鹽水,放置一段時間后看到鐵片上有鐵銹出現。鐵片腐蝕過程中發生的總化學方程式:2Fe+2H2O+O2===2Fe(OH)2,Fe(OH)2進一步被氧氣氧化為Fe(OH)3,再在一定條件下脫水生成鐵銹,其原理如圖。下列說法正確的是( )

A. 鐵片發生還原反應而被腐蝕
B. 鐵片腐蝕最嚴重區域應該是生銹最多的區域
C. 鐵片腐蝕中負極發生的電極反應:2H2O+O2+4e-===4OH-
D. 鐵片里的鐵和碳與食鹽水形成無數微小原電池,發生了電化學腐蝕
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用如下圖所示裝置來制備乙炔,并驗證乙炔的某些化學性質,制備的 乙炔氣體中往往含有少量的 H2S 氣體,請按下列要求填空:

(1)實驗室制乙炔的化學方程式是:_________________;為了得到較為平穩的乙炔氣流, 裝置 A 的分液漏斗中常用_____來代替水.
(2)裝置 B 中CuSO4溶液的作用是_____.
(3)裝置 D 中觀察到的現象是_____
(4)若稱取m g 電石,反應完全后,測得B處溴的CCl4溶液增重n g,則CaC2的純度為_____(用m與n表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子能在強堿性溶液中大量共存,且溶液為無色透明的是( )
A.K+、MnO4-、Mg2+、Cl-B.Na+、Ba2+、HCO3-、NO3-
C.Na+、NO3-、CO32-、Cl-D.K+、H+、Cl-、SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙炔是一種重要的有機化工原料,以乙炔為原料在不同的反應條件下可以轉化成以下化合物。

完成下列各題:
(1)乙炔在一定條件下制取苯的化學反應方程式是_________________________。
(2)正四面體烷的分子式為___________,其二氯取代產物有__________種。
(3)關于乙烯基乙炔分子的說法正確的是__________。
A.由乙炔通過取代反應制得
B.能使酸性KMnO4溶液褪色
C.1 mol乙烯基乙炔能與3 mol Br2發生加成反應
D.等物質的量的乙炔與乙烯基乙炔完全燃燒時的耗氧量相同
(4)寫出與環辛四烯互為同分異構體且屬于芳香烴的分子的結構簡式有_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生活中應注重食譜營養搭配的均衡性,下列午餐食譜中最有利于學生身體發育的是
A. 饅頭、榨菜、黃瓜、香蕉
B. 面條、醋溜土豆絲、素炒白菜
C. 米飯、糖醋排骨、粉蒸肉、清蒸鱸魚
D. 米飯、紅燒鯽魚、西紅柿蛋湯、蒜蓉生菜、蘋果
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com