
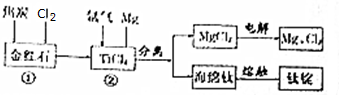
分析 金紅石中加入焦炭,通入氯氣發生反應生成TiCl4,同時生成CO,在TiCl4中通入氬氣、氯氣,得到Ti、MgCl2,電解氯化鎂可的得到鎂,海綿鈦經熔融可得到鈦錠,
(1)反應①通常在800~900℃的條件下進行,反應的方程式為2C+2Cl2+TiO2$\frac{\underline{\;800-900℃\;}}{\;}$2CO+TiCl4,結合方程式計算;
(2)用Mg還原TiCl4制金屬鈦取過程中必須在1070K的溫度下進行,而在此溫度下鎂、鈦都會與氧氣反應;金屬鈦中混有少量雜質鎂,由題給信息知鈦的化學活性很小,僅能與氧氣等幾種物質起反應,而與稀鹽酸或稀硫酸等不反應;
(3)流程中用到Mg、Cl2,電解氯化鎂可生成Mg、Cl2,則二者可循環使用.
解答 解:金紅石中加入焦炭,通入氯氣發生反應生成TiCl4,同時生成CO,在TiCl4中通入氬氣、氯氣,得到Ti、MgCl2,電解氯化鎂可的得到鎂,海綿鈦經熔融可得到鈦錠,
(1)反應①通常在800~900℃的條件下進行,反應的方程式為2C+2Cl2+TiO2$\frac{\underline{\;800-900℃\;}}{\;}$2CO+TiCl4,反應中C為還原劑,1mol Cl2完全反應時,有1molC參加反應,故答案為:1;
(2)用Mg還原TiCl4制金屬鈦取過程中必須在1070K的溫度下進行,而在此溫度下鎂、鈦都會與氧氣反應,所以反應過程中通入氬氣的目的是防止Mg在高溫下與空氣中O2、CO2等反應,金屬鈦中混有少量雜質鎂,由題給信息知鈦的化學活性很小,僅能與氧氣等幾種物質起反應,而與稀鹽酸或稀硫酸等不反應,所以實驗操作為①加入過量的稀鹽酸②過濾③洗滌、干燥固體,
故答案為:防止Mg在高溫下與空氣中O2、CO2等反應;①加入過量的稀鹽酸②過濾③洗滌、干燥固體;
(3)流程中用到Mg、Cl2,電解氯化鎂可生成Mg、Cl2,則二者可循環使用,故答案為:Mg、Cl2.
點評 本題考查物質的制備實驗方案的設計,側重于學生的分析能力和實驗能力的考查,為高考常見題型,難度中等,注意把握實驗的基本原理和物質的性質.


 孟建平小學滾動測試系列答案
孟建平小學滾動測試系列答案 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案科目:高中化學 來源: 題型:實驗題
 現使用酸堿中和滴定法測定市售白醋的濃度.
現使用酸堿中和滴定法測定市售白醋的濃度.次數 數據(mL) | 1 | 2 | 3 |
| V(樣品) | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 14.95 | 16.05 | 15.95 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 液化石油氣和天然氣的主要成分都是甲院 | |
| B. | 苯、乙醇和乙酸都能發生取代反應 | |
| C. | 油脂在堿的催化作用下可發生水解,工業上利用該反應生產肥皂 | |
| D. | 煤的氣化是化學變化,石油分餾是物理變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
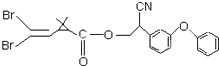 擬除蟲菊酯是一類高效、低毒的殺蟲劑,其中對光穩定的溴氰菊酯的結構簡式如圖所示,下列對該化合物的敘述中,正確的是( )
擬除蟲菊酯是一類高效、低毒的殺蟲劑,其中對光穩定的溴氰菊酯的結構簡式如圖所示,下列對該化合物的敘述中,正確的是( )| A. | 屬于芳香烴 | B. | 每一個分子內含23個碳原子 | ||
| C. | 屬于高分子化合物 | D. | 每一個分子內含7個碳碳雙鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 容器 | 甲 | 乙 | 丙 |
| 反應物投入量 | 2molSO2、1molO2 | 1molSO2、0.5molO2 | 2molSO3 |
| k1 | k2 | k3 | |
| 反應的能量變化 | 放出akJ | 放出bkJ | 吸收ckJ |
| 氣體密度 | ρ1 | ρ2 | ρ3 |
| 反應物轉化率 | α1 | α2 | α3 |
| A. | k1=k3<k2 | B. | ρ1=ρ3>ρ2 | C. | α2+α3>1 | D. | 2b+c>197 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com