
X、Y、Z、P、Q、W、R、T是元素周期表短期中最常見的主族元素,且原子序數依次增大,其相關信息如下表:
元素 | 相關信息 |
X | 某一種同位素,可被用作相對原子質量的標準 |
Y | 其最高價氧化物對應水化物能與其氣態氫化物相互間發生化合反應 |
P | 是短周期中(除稀有氣體外)原子半徑最大的元素 |
Q | 存在質量數為25,中子數為13的核素 |
W | 位于周期表第13列 |
R | 與Z同族,且最高價氧化物對應水化物的濃溶液常溫下與W單質會出現鈍化現象 |
(1)R在元素周期表中的位置為__________;將Q、W、Z、Y的簡單離子的半徑從大到小排序__________________________(用離子符號表示)
(2)T的單質易溶于XT4中,理由是______________________________________。
(3)根據下表中的信息,判斷下列化合物固態的晶體類型(填“離子晶體”……等);)
化合物 | X3Y4 | R2T2 |
晶體類型 |
|
|
熔點/°C | >3600 | -76 |
(4)任意寫出一個由Y、Z元素分別與氫元素形成的10電子粒子間相互反應的離子方程式:
_________________________________________________________________________。
(5)在25°C、10kPa下,已知13.5g的W固體單質在Z2氣體中完全燃燒后恢復至原狀態,放熱419kJ,寫出表示W單質燃燒熱的熱化學方程式______________________________。
(6)化合物P2R溶液在空氣中長期放置,與氧氣反應會生成與過氧化鈉的結構相似的物質P2R2,其溶液顯黃色,則P2R2的電子式為___________,用化學方程式表示P2R溶液在空氣中的變質過程________.
科目:高中化學 來源:2015-2016學年江西省高一下學期期末考試化學試卷(解析版) 題型:選擇題
某新型電池,以NaBH4(B的化合價為+3價)和H2O2作原料,該電池可用作深水勘探等無空氣環境電源,其工作原理如圖所示。下列說法正確的是( )
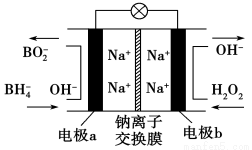
A.電池工作時Na+從b極區移向a極區
B.每消耗3 mol H2O2,轉移3 mol e-
C.b極上的電極反應式為H2O2+2e-+2H+===2H2O
D.a極上的電極反應式為BH4-+8OH--8e-===BO2-+6H2O
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省揚州市高二選修下學期期末調研化學試卷(解析版) 題型:填空題
科學研究與工業生產中常常用到溶液中的反應。
(1)25℃時,0.05 mol·L-1Ba(OH)2溶液的pH= ,將該Ba(OH)2溶液與pH=2的HCl溶液混合,若所得混合溶液pH=7,則Ba(OH)2溶液與HCl溶液的體積比為 。
(2)CO2可轉化成有機物實現碳循環:CO2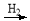 CH3OH
CH3OH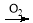 HCOOH……
HCOOH……
25 ℃時,幾種酸的電離平衡常數如下:
化學式 | HCOOH | H2CO3 | HClO |
電離平衡常數 | 1.7×10-4 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列問題:
①用離子方程式表示HCOONa溶液呈堿性的原因 。
②物質的量濃度均為0.1 mol·L-1的下列四種物質:
a.Na2CO3 b.NaClO c.HCOONa d.NaHCO3 ,pH由大到小的順序是 (填編號)。
(3)常溫下,將0.2 mol·L-1的HCOOH和0.1 mol·L-1的NaOH溶液等體積混合,所得溶液的pH<7,說明所得混合溶液中HCOOH的電離程度 HCOONa的水解程度(填“大于”“等于”或“小于”)。
(4)含有Cr2O72-的廢水毒性較大,某工廠廢水中含5.00×10-3 mol·L-1的Cr2O72-。為使廢水能達標排放,做如下處理:Cr2O72-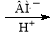 Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3。若處理后的廢水中殘留的c(Fe3+)=2×10-13 mol·L-1,則殘留的Cr3+的濃度為 mol·L-1 (已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
Cr(OH)3、Fe(OH)3。若處理后的廢水中殘留的c(Fe3+)=2×10-13 mol·L-1,則殘留的Cr3+的濃度為 mol·L-1 (已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南省懷化市高一下學期期末考試化學試卷(解析版) 題型:選擇題
下列物質中,屬于共價化合物的是
A.H2 B.HCl C.NaCl D.NaOH
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南省懷化市高一下學期期末考試化學試卷(解析版) 題型:選擇題
在元素周期表中,同主族元素原子具有相同的
A. 電子層數 B. 核電荷數
C. 核外電子數 D. 最外層電子數
查看答案和解析>>
科目:高中化學 來源:2015-2016學年重慶一中高一下期末化學試卷(解析版) 題型:選擇題
關于如圖所示轉化關系(X代表鹵素),說法正確的是
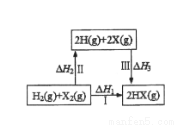
A.H2(g)+X2(g)=2H(g)+2X(g);△H2>0
B.生成HX的反應熱與途徑有關,所以△H1≠△H2+△H3
C.若X分別表示Cl,Br,I,則過程Ⅱ吸收的熱量依次增多
D.△H1代表H2的燃燒熱
查看答案和解析>>
科目:高中化學 來源:2015-2016學年重慶一中高一下期末化學試卷(解析版) 題型:選擇題
下列各組性質的比較中,不正確的是
A. 堿性:NaOH>Mg(OH)2
B. 熱穩定性:HCl>HBr
C. 失電子能力:K>Na
D. 原子半徑:Cl>S
查看答案和解析>>
科目:高中化學 來源:2015-2016學年陜西西安高新一中高一下期末化學試卷(解析版) 題型:選擇題
下列圖示與對應的敘述相符的是
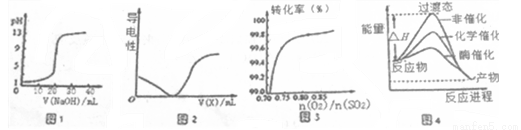
A.圖一表示0.1000mol·L-1NaOH溶液滴定20.00ml 0.1000 mol·L-1醋酸溶液得到滴定曲線
B.圖2所示在H2S溶液導電性實驗中,曲線可確定通入的氣體X為Cl2
C.圖3在其它條件不變時,2SO2(g)+O2(g)  2SO3(g)轉化關系中,縱坐標表示O2的轉化率
2SO3(g)轉化關系中,縱坐標表示O2的轉化率
D.由圖4所示曲線可知,酶催化比化學催化的效果好
【答案】D
【解析】
試題分析:A.醋酸是弱酸,0.1mol/L的醋酸的pH>1,所以圖一表示0.1000mol·L-1NaOH溶液滴定20.00ml 0.1000 mol·L-1一元強酸溶液得到滴定曲線,錯誤;B.在H2S的溶液中通入Cl2,會發生反應:Cl2+H2S=S↓+2HCl,溶液的酸性增強,離子濃度增大,溶液的導電性增強,與圖像不吻合,錯誤;C.2SO2(g)+O2(g)  2SO3(g)是可逆反應,在其它條件不變時,增大氧氣的濃度,化學平衡正向移動,但是O2的轉化率會降低,不符合圖像,錯誤;D.催化劑可以降低反應的活化能,使反應速率加快,反應需要的活化能越低,反應速率就越快。根據圖示可知酶催化比化學催化的效果好,正確。
2SO3(g)是可逆反應,在其它條件不變時,增大氧氣的濃度,化學平衡正向移動,但是O2的轉化率會降低,不符合圖像,錯誤;D.催化劑可以降低反應的活化能,使反應速率加快,反應需要的活化能越低,反應速率就越快。根據圖示可知酶催化比化學催化的效果好,正確。
考點:考查圖像方法在溶液的導電性、化學反應及催化劑的作用比較的應用的知識。
【題型】選擇題
【適用】較難
【標題】【百強校】2015-2016學年陜西西安高新一中高一下期末化學試卷(帶解析)
【關鍵字標簽】
【結束】
已知:① 2CO(g)+O2(g) 2CO2(g) △H=-566kJ/mol;
2CO2(g) △H=-566kJ/mol;
②Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) △H=-226kJ/mol
根據以上熱化學方程式判斷,下列說法正確的是

A.CO(g)與Na2O2(s)反應放出509kJ熱量時,消耗的CO是28g
B.如上圖可表示由CO生成CO2的反應過程和能量關系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H<-452 kJ/mol
D.CO的燃燒熱為-566 kJ/mol
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高一下期末化學試卷(解析版) 題型:選擇題
下列化學用語書寫正確的是
A.用電子式表示氫溴酸的形成過程為: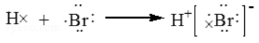
B.乙烯的結構簡式:C2H4
C.四氯化碳的電子式為: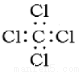
D.質子數為27、中子數為33的Co原子: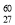 Co
Co
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com