
| A. | 標準狀況下,22.4L乙烯含有的共用電子對數為2N0 | |
| B. | 常溫下,含有1 mo1 NaHSO4的溶液中陽離子數為N0 | |
| C. | 通常狀況下,1 mo1 NO和0.5 mo1 O2在密閉容器中混合,生成NO2分子數為N0 | |
| D. | 制取漂白粉時,標準狀況下22.4 L Cl2參加反應,轉移電子數為N0 |
分析 A、乙烯中含6對共用電子對;
B、NaHSO4在溶液中能完全電離為鈉離子、氫離子和硫酸根;
C、在NO2氣體中存在平衡:2NO2?N2O4;
D、在制取漂白粉的反應中,氯氣發生歧化反應.
解答 解:A、乙烯中含6對共用電子對,故標況下22.4L乙烯即1mol乙烯中含6mol共用電子對即6N0個,故A錯誤;
B、NaHSO4在溶液中能完全電離為鈉離子、氫離子和硫酸根,故含有1 mo1 NaHSO4的溶液中陽離子數為2N0,故B錯誤;
C、1 mo1 NO和0.5 mo1 O2在密閉容器中混合生成1molNO2,而在NO2氣體中存在平衡:2NO2?N2O4,導致分子個數小于N0個,故C錯誤;
D、在制取漂白粉的反應中,氯氣發生歧化反應,故標況下22.4L氯氣即1mol氯氣反應時轉移1mol電子即N0個,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 混合氣體中一定沒有乙炔 | B. | 混合氣體中一定有乙稀 | ||
| C. | 混合氣體可能由乙炔和丙烯組成 | D. | 混合氣體一定由乙烯和乙炔組成 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
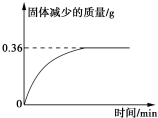 礦物透閃石是制作玉器的一種原料,其化學式可用CaxMgySi8O22(OH)m表示.
礦物透閃石是制作玉器的一種原料,其化學式可用CaxMgySi8O22(OH)m表示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石油、沼氣、天然氣、植物油都屬于可再生能源 | |
| B. | 應用蓋斯定律,可計算某些難以直接測量的反應焓變 | |
| C. | 水蒸氣變為液態水時放出的能量就是該變化的反應熱 | |
| D. | 同溫同壓下,H2(g)+Cl2(g)═2HCl(g)在光照和點燃條件下的△H不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子式為C5H10的有機化合物全都能使溴水褪色 | |
| B. | 相同條件下,等質量的碳按a、b 兩種途徑完全轉化,途徑a 比途徑b 放出更多熱能 途徑a:C$→_{高溫}^{H_{2}O}$CO+H2O$→_{燃燒}^{O_{2}}$CO2 途徑b:C$→_{燃燒}^{O_{2}}$CO2 | |
| C. | 淀粉和纖維素水解的最終水解產物相同 | |
| D. | 若H2O2分解產生1molO2,理論上轉移的電子數約為4×6.02×1023 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
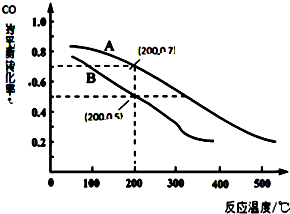 科學家開發出一種“潔凈煤技術”,通過向地下煤層“氣化爐”中交替鼓入空氣和水蒸氣的方法,連續產出高熱值的煤炭氣,其主要成分是CO和H2.“氣化爐”中主要反應有:
科學家開發出一種“潔凈煤技術”,通過向地下煤層“氣化爐”中交替鼓入空氣和水蒸氣的方法,連續產出高熱值的煤炭氣,其主要成分是CO和H2.“氣化爐”中主要反應有:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 在一定溫度和壓強條件下發生了反應:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,反應達到平衡時,改變溫度(T)和壓強(p),反應混合物CH3OH“物質的量分數”變化情況如圖所示,關于溫度(T)和壓強(p)的關系判斷正確的是( )
在一定溫度和壓強條件下發生了反應:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,反應達到平衡時,改變溫度(T)和壓強(p),反應混合物CH3OH“物質的量分數”變化情況如圖所示,關于溫度(T)和壓強(p)的關系判斷正確的是( )| A. | P3>P2T3>T2 | B. | P2>P4T4>T2 | C. | P1>P3T3>T1 | D. | P1>P4T2>T3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放電時Pb極為負極 | |
| B. | 充電時蓄電池上標有“+”號電極連接電源正極 | |
| C. | 放電時正極反應為PbO2+SO42-+4H++2e═PbSO4+2H2O | |
| D. | 充電時蓄電池上標有“-”號的電極發生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 摩爾是一種物理量 | |
| B. | 溶液中或熔融狀態下能導電的物質就是電解質 | |
| C. | 氧化還原反應的本質是元素化合價發生了變化 | |
| D. | 得電子的物質被還原,是氧化劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com