
| A. | 4FeS2( s)+11O2( g)═2Fe2O3( s)+8SO2(g)△H=-3414.8kJ•moL | |
| B. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=-853.7kJ•moL | |
| C. | 4FeS2(s)+11O2(g)═2 Fe2O3 (s)+8SO2(g)△H+3414.8kJ•moL | |
| D. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=+853.7kJ•moL |
分析 101kPa時燃燒1t含FeS2質量分數為70%的黃鐵礦生成固態Fe2O3和氣態SO2,放出4.98×106 kJ的熱量,則燃燒120g即1molFeS2會放出熱量為:$\frac{120×4.98×1{0}^{6}}{1{0}^{6}×70%}$kJ=853.7kJ,即FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3(s)+2SO2(g);△H=-853.7kJ•mol-1,據此進行解答.
解答 解:101kPa時燃燒1t含FeS2質量分數為70%的黃鐵礦生成固態Fe2O3和氣態SO2,放出4.98×106 kJ的熱量,則燃燒120g即1molFeS2會放出熱量為:$\frac{120×4.98×1{0}^{6}}{1{0}^{6}×70%}$kJ=853.7kJ,即FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3(s)+2SO2(g);△H=-853.7kJ•mol-1,
A.4molFeS2(s)完全反應放出熱量為853.7kJ×4=3414.8kJ,則反應的熱化學方程式為:4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g);△H=-3414.8kJ•mol-1,故A正確;
B.根據分析可知,反應的熱化學方程式為:FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3(s)+2SO2(g);△H=-853.7kJ•mol-1,故B正確;
C.該反應為放熱反應,焓變值應該小于0,故C錯誤;
D.該反應為放熱反應,焓變△H<0,故D錯誤;
故選AB.
點評 本題主要考查了熱化學方程式的書寫,題目難度不大,需要注意熱化學方程式中物質的狀態、反應熱的數值與單位,反應熱的數值與化學方程式前面的系數成正比.


 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:高中化學 來源: 題型:多選題
| A. | Fe | B. | Mg | C. | Al | D. | Zn |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol任何物質都含有6.02×1021個原子, | |
| B. | 0.012kg12C含有6.02×1023碳原子 | |
| C. | 阿伏伽德羅常數表示的粒子“集體”就是1mol | |
| D. | 使用摩爾這一單位時必須指明粒子的名稱 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
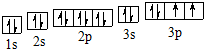 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
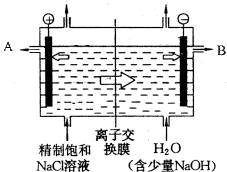 工業上電解制燒堿的技術是用離子交換膜法,主要原料是飽和食鹽水.圖為離子交換膜法電解原理示意圖:
工業上電解制燒堿的技術是用離子交換膜法,主要原料是飽和食鹽水.圖為離子交換膜法電解原理示意圖:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 某固體酸燃料電池以CsHSO4固體為電解質傳遞H+,其基本結構見如圖,電池總反應可表示為:2H2+O2═2H2O,下列有關說法正確的是( )
某固體酸燃料電池以CsHSO4固體為電解質傳遞H+,其基本結構見如圖,電池總反應可表示為:2H2+O2═2H2O,下列有關說法正確的是( )| A. | 電子通過外電路從b極流向a極 | |
| B. | b極上的電極反應式為:O2+4H++4e-═2H2O | |
| C. | 每轉移0.1mol電子,消耗1.12L的H2 | |
| D. | H+由b極通過固體酸電解質傳遞到a極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C(Na+)>C(Ac-)=C(OH-)>C(H+) | B. | C(Na+)>C(Ac-)>C(OH-)>C(H+) | ||
| C. | C(Na+)=C(Ac-)+C(HAc) | D. | C(Na+)+C(H+)=C(Ac-)+C(OH) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com