
分析 (1)根據準確配制一定體積一定物質的量濃的溶液用到的儀器來回答;
(2)殘缺方程式配平首先確定缺什么,根據電子轉移守恒,配平化學方程式;
(3)酸式滴定管可以量取具有強氧化性的溶液,高錳酸鉀具有顏色,錳離子無色;
(4)根據化學方程式計算消耗過氧化氫的量然后計算質量分數;
(5)滴定實驗中誤差分析依據消耗標準溶液的體積變化判斷產生誤差的結果,
c(待測)=$\frac{c(標準)V(標準)}{V(待測)}$,若標準溶液消耗體積越大,測定結果越高;
A.若將錐形瓶用蒸餾水潤洗后未用待測液潤洗對測定結果無影響;
B.滴定管用蒸餾水洗后未用標準液潤洗,導致標準溶液濃度減小;
C.若滴定前滴定管尖嘴中有氣泡,滴定后氣泡消失,則有一部分溶液占據了氣泡的體積
D.滴定前平視讀數,滴定結束俯視讀數,消耗標準溶液體積減小.
解答 解:(1)準確配制一定體積一定物質的量濃的溶液用250ml容量瓶,故答案為:容量瓶;
(2)方程式中,高錳酸鉀有強氧化性,能將雙氧水氧化為氧氣,先確定缺的是O2,錳元素化合價降低了5價,生成1mol氧氣時,氧元素化合價升高2價,根據電子轉移守恒,配平化學方程式高錳酸根前面的系數為2,雙氧水前面的系數為5,根據原子守恒來配平其他物質前面的系數,離子方程式2MnO4-+5H2O2+6H+=2Mn2++8H2O+502↑,
故答案為:2、5、6、2、8、502;
(3)由于高錳酸鉀標準溶液具有強氧化性,所以只能使用酸式滴定管,滴定到達終點的現象是:滴入一滴高錳酸鉀溶液,溶液呈淺紅色,且30秒內不褪色,
故答案為:酸式;滴入一滴高錳酸鉀溶液,溶液呈淺紅色,且30秒內不褪色;
(4)根據化學方程式可以得到關系式:2MnO4-~5H2O2,耗用c mol/L KMnO4標準溶液V mL,即cV×10-3mol的高錳酸鉀時,所用雙氧水的物質的量:2.5cV×10-3mol,則原過氧化氫的質量為:0.025cVmol×34g/mol=0.85cV,過氧化氫溶液中過氧化氫的質量分數為:$\frac{0.85cV}{10.00ml×ρg/mol}$×100%=$\frac{17cV}{200ρ}$×100%,
故答案為:$\frac{17cV}{200ρ}$×100%;
(5)A.若將錐形瓶用蒸餾水潤洗后未用待測液潤洗,待測液溶質物質的量不變,對測定結果無影響,故A錯誤;
B.滴定管用蒸餾水洗后未用標準液潤洗,導致標準溶液濃度減小,測定濃度偏低,故B正確;
C.若滴定前滴定管尖嘴中有氣泡,滴定后氣泡消失,有一部分溶液占據了氣泡的體積,并沒有滴入錐形瓶,則測定結果偏高,故C正確;
D.觀察酸式滴定管液面時,開始平視,滴定終點俯視,消耗標準溶液體積減小,測定結果偏低,故D錯誤;
故答案為:BC.
點評 本題是一道綜合知識題目,考查角度廣,考查了物質組成和含量的實驗測定,主要是滴定實驗的步驟和有關計算,氧化還原反應化學方程式配平等知識點,要求學生具有分析和解決問題的能力,題目難度中等.


科目:高中化學 來源: 題型:解答題
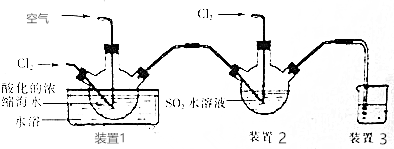
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗次數編號 | 鹽酸溶液體積V(mL) | 氫氧化鈉溶液體積 V(mL) |
| 1 | 22.4 | 10.00 |
| 2 | 22.60 | 10.00 |
| 3 | 26.00 | 10.00 |
| 4 | 22.50 | 10.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 氫化物 | A | B | HF | D | E |
| 沸點/℃ | 1317 | 100 | 19.5 | -33.35 | -164 |
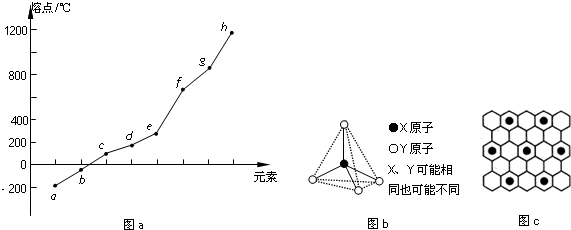
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.2 mol•L-1醋酸溶液與 0.1 mol•L-1醋酸溶液中c(H+)之比 | |
| B. | (NH4)2SO4溶液中c(NH4+)和c(SO42-)的物質的量濃度之比 | |
| C. | pH=2的鹽酸和pH=12的Ba(OH)2溶液中溶質的物質的量濃度之比 | |
| D. | 0.2 mol/LCH3COONa溶液與 0.1 mol•L-1Na2CO3溶液中c(CH3COO-)與c(CO32-)之比 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
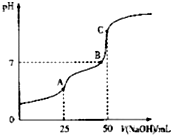 25°C時,向25ml 0.1wol•L-1 H2C2O4溶液中滴加同濃度的NaOH溶液,混合溶液的pH隨滴加NaOH溶液體積的變化如圖所示.下列有關敘述錯誤的是( )
25°C時,向25ml 0.1wol•L-1 H2C2O4溶液中滴加同濃度的NaOH溶液,混合溶液的pH隨滴加NaOH溶液體積的變化如圖所示.下列有關敘述錯誤的是( )| A. | HC2O4-的電離程度大于其水解程度 | |
| B. | B點時溶液中含有NaHC2O4和Na2C2O4 | |
| C. | A點時,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) | |
| D. | C點時,c(Na+)>c(C2O42-)>c(HC2O4-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | 6 | 7 | ||||||
| 3 | 1 | 3 | 5 | 8 | 10 | |||
| 4 | 2 | 4 | 9 |
 H++Cl-+HClO.
H++Cl-+HClO.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
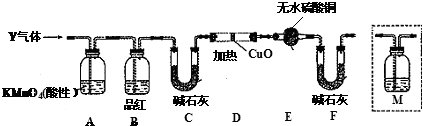
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某課外興趣小組欲測定某NaOH溶液的濃度,其操作步驟如下:①將堿式滴定管用蒸餾水洗凈,待測溶液潤洗后,再注入待測溶液,調節滴定管的尖嘴部分充滿溶液,并使液面處于“0“刻度以下的位置,記下讀數;將錐形瓶用蒸餾水洗凈后,用待測溶液潤洗錐形瓶2~3次;從堿式滴定管中放入20.00mL待測溶液到錐形瓶中.
某課外興趣小組欲測定某NaOH溶液的濃度,其操作步驟如下:①將堿式滴定管用蒸餾水洗凈,待測溶液潤洗后,再注入待測溶液,調節滴定管的尖嘴部分充滿溶液,并使液面處于“0“刻度以下的位置,記下讀數;將錐形瓶用蒸餾水洗凈后,用待測溶液潤洗錐形瓶2~3次;從堿式滴定管中放入20.00mL待測溶液到錐形瓶中.| 滴定次數 | 待測液體積(mL) | 標準鹽酸體積/mL | |
| 滴定前讀數(mL) | 滴定后讀數(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.00 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com