
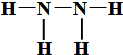
分析 (1)根據焓變等于反應物鍵能之和-生成物鍵能之和計算;
(2)①$\frac{1}{2}$N2(g)+O2(g)═NO2(g)△H1=+33.6kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-543kJ•mol-1
依據蓋斯定律②×2-①×2計算得到.
解答 解:(1)在反應N2H4(g)+O2(g)═N2(g)+2H2O(l)△H2=-534kJ/mol,設N2H4(肼)中N-N的鍵的鍵能為xkJ/mol,則根據焓變等于反應物鍵能之和-生成物鍵能之和,所以△H2=-534kJ/mol=391×4+x+495-946-463×4,解得x=205kJ/mol
故答案為:205;
(2)①$\frac{1}{2}$N2(g)+O2(g)═NO2(g)△H1=+33.6kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-543kJ•mol-1
依據蓋斯定律②×2-①×2得到,2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-543×2-33.6×2=-1153.2kJ•mol-1;
故答案為:2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1153.2kJ•mol-1 .
點評 本題考查了熱化學方程式的計算和蓋斯定律的計算應用,理解實質,掌握基礎是解題關鍵,題目較簡單.


科目:高中化學 來源: 題型:多選題
| A. | FeCl3溶液與Cu粉反應:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 鈉與水反應:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 氯氣與水反應:Cl2+H2O?2H++Cl-+ClO- | |
| D. | 氯化鋁溶液與過量氨水反應:3NH3•H2O+Al3+=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某研究性學習小組設計了一組實驗,驗證元素周期律.
某研究性學習小組設計了一組實驗,驗證元素周期律.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
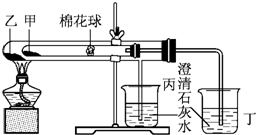 下列是某興趣小組根據課本實驗設計的一個能說明碳酸鈉與碳酸氫鈉熱穩定性的套管實驗.請觀察下圖的實驗裝置,分析實驗原理,回答下列問題:
下列是某興趣小組根據課本實驗設計的一個能說明碳酸鈉與碳酸氫鈉熱穩定性的套管實驗.請觀察下圖的實驗裝置,分析實驗原理,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH4分子的比例模型: | B. | 氯原子的結構示意圖: | ||
| C. | NH3分子的電子式: | D. | CO2分子的結構式:O=C=O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
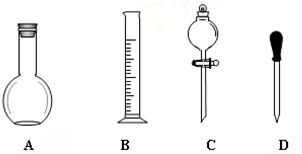 實驗室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根據這兩種溶液的配制情況回答下列問題.
實驗室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根據這兩種溶液的配制情況回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含有NA個氦原子的氦氣在標準狀況下的體積約為11.2L | |
| B. | 標準狀況下,9克H2O 含有的分子數為0.5NA | |
| C. | 常溫常壓下,32g O2和O3的混合氣體所含原子數為2NA | |
| D. | 1mol Fe和足量稀鹽酸反應,鐵失去的電子數為2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com