
| A. | 升高反應的溫度,活化分子百分數增加,有效碰撞的幾率提高,反應速率增大 | |
| B. | 活化分子的碰撞一定是有效碰撞 | |
| C. | 增大反應物的濃度,活化分子百分數增加,反應速率加快 | |
| D. | 催化劑不影響反應活化能但能增大單位體積內活化分子百分數,從而增大反應速率 |
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碘易溶于四氯化碳,甲烷難溶于水都可用相似相溶原理解釋 | |
| B. | 乳酸[CH3CH(OH)COOH]中存在一個手性碳原子 | |
| C. | 許多過渡金屬離子對多種配體具有很強的結合力,因而,只有過渡金屬才能形成配合物 | |
| D. | 已知酸性:H3PO4>HClO,是因為H3PO4分子中有1個非羥基氧原子為0 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
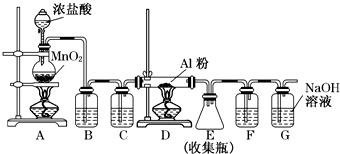
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.8 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.8 mol |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上第一次月考化學卷(解析版) 題型:填空題
某反應的△H=+100kJ·mol-1,以下有關該反應的敘述正確是_________
①正反應活化能小于100kJ·mol-1
②逆反應活化能一定小于100kJ·mol-1
③正反應活化能不小于100kJ·mol-1
④正反應活化能比逆反應活化能大100kJ·mol-1
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上第一次月考化學卷(解析版) 題型:選擇題
可逆反應2SO2(g)+O2(g)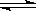 2SO3(g)從正方向開始,并達到了平衡。此時SO2和O2的物質的量之比為2∶1;若采取某種措施,導致SO2和O2又消耗了一些,并再次達到平衡,下列說法正確的是( )
2SO3(g)從正方向開始,并達到了平衡。此時SO2和O2的物質的量之比為2∶1;若采取某種措施,導致SO2和O2又消耗了一些,并再次達到平衡,下列說法正確的是( )
A .新平衡體系中,SO2和O2物質的量之比仍為2∶1
B .平衡向正反應方向移動了,原因是正反應速率增大了,逆反應速率減小了
C .新平衡體系與舊平衡體系比較,SO3的濃度肯定增大了
D .若采取的措施是縮小容器的容積,則新舊平衡中SO2和O2的轉化率之比都是1∶1
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氟氯代烷--臭氧空洞--皮膚癌患者增多 | |
| B. | 汽車尾氣--光化學污染--咳嗽和氣喘患者增多 | |
| C. | 人口增多--空氣中CH4的濃度增大--溫室效應 | |
| D. | 含磷洗衣粉--水體富營養化--水棲生物大量死亡 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
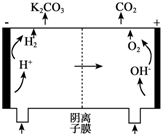 為實現CO2減排,熱鉀堿法化學吸收CO2在合成氨、制氫、天然氣等石油化工行業中應用廣泛.該方法的原理是用碳酸鉀溶液吸收CO2生成碳酸氫鉀(稱富液)來脫除CO2.之后高溫加熱富液,使碳酸氫鉀分解釋放CO2生成碳酸鉀,溶液循環使用.某研究小組用500mL 1mol/L K2CO3溶液吸收5.6L 的CO2(標準狀況)形成富液(忽略溶液體積變化).
為實現CO2減排,熱鉀堿法化學吸收CO2在合成氨、制氫、天然氣等石油化工行業中應用廣泛.該方法的原理是用碳酸鉀溶液吸收CO2生成碳酸氫鉀(稱富液)來脫除CO2.之后高溫加熱富液,使碳酸氫鉀分解釋放CO2生成碳酸鉀,溶液循環使用.某研究小組用500mL 1mol/L K2CO3溶液吸收5.6L 的CO2(標準狀況)形成富液(忽略溶液體積變化).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com