

分析 含有Cr2O72-和CrO42-的廢水經酸化后主要轉化為Cr2O72-,Cr2O72-具有強氧化性,加入還原性的亞鐵離子,將其還原為Cr3+,本身被氧化成Fe3+,然后依據溶度積常數調節pH1使Fe3+沉淀,過濾得沉淀C為Fe(OH)3,濾液含Cr3+,再依據溶度積常數調節pH2使Cr3+沉淀,據此分析解答;
(1)根據2CrO42-(黃色)+2H+?Cr2O72-(橙色)+H2O,酸化平衡正向移動分析;
(2)防止亞鐵離子氧化,還要抑制亞鐵離子水解,據此解答即可;
(3)亞鐵離子具有還原性,鉻酸根具有強氧化性,據此書寫離子反應方程式即可;
(4)根據以上分析,沉淀C的化學式為Fe(OH)3;當離子濃度小于1.0×10-5 mol•L-1時,認為沉淀完全,據此解答即可.
解答 解:(1)因為2CrO42-(黃色)+2H+?Cr2O72-(橙色)+H2O,所以酸化平衡正向移動,則酸化后的溶液A顯橙色;故答案為:橙;
(2)防止亞鐵離子氧化,并抑制水解,則配制FeSO4溶液時,需加入少量鐵粉和稀硫酸,
故答案為:鐵粉、硫酸;
(3)依據分析可知:溶液A含有Cr2O72-,具有強氧化性,能氧化亞鐵離子為鐵離子,離子反應方程式為:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,故答案為:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
(4)根據以上分析,沉淀C的化學式為Fe(OH)3;當離子濃度小于1.0×10-5 mol•L-1時,認為沉淀完全,故鉻離子完全沉淀時有:1×10-5×c(OH)3=1.0×10-32,解得c(OH)=$\root{3}{\frac{1.0×10{\;}^{-32}}{1×10{\;}^{-5}}}$=10-9,即pH≥5完全沉淀,所以要使Cr3+沉淀完全pH2值至少為5,故答案為:Fe(OH)3;5.
點評 本題主要考查的是金屬的回收與資源利用,涉及氧化還原反應、化學反應平衡移動原理、離子反應方程式書寫等,難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Na+、NO3-、SO42- | B. | K+、Na+、Cl-、Cr2O42- | ||
| C. | Al3+、K+、AlO2-、Cl- | D. | Fe3+、NO3-、SO42-、NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol Al3+離子含有的核外電子數為3NA | |
| B. | 1molCl2與足量的鐵反應,轉移的電子數為3NA | |
| C. | 10 LpH=l的硫酸溶液中含有的H+離子數為NA | |
| D. | 1L0.5mol/L的碳酸鈉溶液中含有的CO32-離子數為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| AgNO3 | Ba(NO3)2 | AgCl | BaC12 | |
| H2O (液) | 170g | 9.2g | 1.5×10-4g | 33.3g |
| NH3(液) | 86g | 97.2g | 0.8g | 0g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
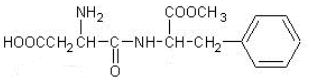
| A. | 分子式為C14H19N2O5 | B. | 既能與酸反應又能與堿反應 | ||
| C. | 不能發生水解反應 | D. | 1mol該物質最多可與2molNaOH反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,0.1molCl2溶于水,轉移的電子數目為0.1NA | |
| B. | 1.0L0.1 mol•L-1 AlCl3溶液中所含的Al3+離子數為0.1NA | |
| C. | 標準狀況下,11.2LSO3中含有分子數目為0.5NA | |
| D. | 常溫常壓下,3.2gO2和O3混合氣體中含有的氧原子數目為0.2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com