
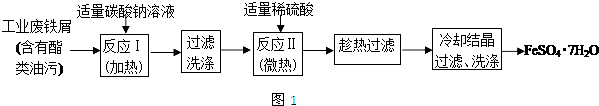

分析 廢鐵屑中含有酯類油污,Na2CO3為強堿弱酸鹽,CO32-水解生成HCO3-和OH-,升高促進CO32-水解,堿促進油脂水解,然后過濾洗滌,加入稀硫酸,發生反應II為Fe+H2SO4=FeSO4+H2↑,趁熱過濾、冷卻結晶,過濾洗滌得到FeSO4•7H2O;
將補血劑研細,向藥片中加入稀硫酸,然后過濾得到沉淀,向濾液中加入雙氧水,發生反應2Fe2++H2O2+2H+=2Fe3++2H2O,向溶液中加入過量X溶液生成紅褐色沉淀,則X為堿,反應的離子方程式為:Fe3++3OH-=Fe(OH)3↓;將紅褐色沉淀灼燒得到紅棕色固體Fe2O3,據此分析解答.
解答 解:廢鐵屑中含有酯類油污,Na2CO3為強堿弱酸鹽,CO32-水解生成HCO3-和OH-,升高促進CO32-水解,堿促進油脂水解,然后過濾洗滌,加入稀硫酸,發生反應II為Fe+H2SO4=FeSO4+H2↑,趁熱過濾、冷卻結晶,過濾洗滌得到FeSO4•7H2O,
(1)Na2CO3為強堿弱酸鹽,CO32-水解生成HCO3-和OH-,水解方程式為CO32-+H2O?HCO3-+OH-,油脂在堿性條件下水解生成可溶于水的酸和醇;
鹽的水解為吸熱反應,升溫,促進水解,溶液堿性增強,使反應充分進行,
故答案為:CO32-+H2O?HCO3-+OH-;升溫,促進水解,溶液堿性增強,使反應充分進行;
(2)廢鐵屑中含氧化鐵,無需在制備前除去,因為氧化鐵和酸反應生成鐵鹽,鐵鹽能被Fe還原生成亞鐵鹽,涉及的離子方程式為Fe2O3+6H+═2Fe3++3H2O、2Fe3++Fe═3Fe2+,
故答案為:Fe2O3+6H+═2Fe3++3H2O、2Fe3++Fe═3Fe2+;
將補血劑研細,向藥片中加入稀硫酸,然后過濾得到沉淀,向濾液中加入雙氧水,發生反應2Fe2++H2O2+2H+=2Fe3++2H2O,向溶液中加入過量X溶液生成紅褐色沉淀,則X為堿,反應的離子方程式為:Fe3++3OH-=Fe(OH)3↓;將紅褐色沉淀灼燒得到紅棕色固體Fe2O3,
(3)步驟Ⅲ需要100mL1mol/L的稀硫酸,用98%,ρ=1.84g/cm3的濃硫酸配制,配制過程中硫酸的物質的量不變,設需要濃硫酸體積為VmL,則:1.84g/cm3×
98%×VmL=98g/mol×1mol/L×0.1L,解得:V=5.4;
配制一定物質的量濃度的溶液時還需要100mL容量瓶;驟Ⅳ的離子方程式為:Fe3++3OH-=Fe(OH)3↓,
故答案為:5.4;100mL容量瓶;Fe3++3OH-=Fe(OH)3↓;
(4)步驟Ⅴ一系列操作依次是:①過濾②洗滌③灼燒④冷卻⑤稱量⑥恒重操作,操作⑥恒重后可確保氫氧化鐵完全分解成了氧化鐵,從而減小誤差,
故答案為:灼燒(加熱);確保氫氧化鐵完全分解成了氧化鐵;
(5)ag中含有鐵的質量為:m(Fe)=$\frac{112}{160}$×ag=0.7ag,則每片藥品中Fe的質量為:$\frac{0.7ag}{10}$=0.07ag,
故答案為:0.07a.
點評 本題考查物質的分離和提純、物質含量的測定,題目難度中等,明確實驗目的、實驗原理為解答關鍵,注意掌握物質分離與提純方法,試題側重考查學生的分析、理解能力及化學實驗能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 氯氣的水溶液可以導電,說明氯氣是電解質 | |
| B. | 漂白粉和明礬都常用于自來水的處理,二者的作用原理是相同的 | |
| C. | 氯氣可以使濕潤的有色布條褪色,但實際起漂白作用的物質是次氯酸而不是氯氣 | |
| D. | 氯水中加入紅色鮮花,紅花褪色,說明溶液中有Cl2存在 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 1 mol磷酸鉀中陰離子所帶電荷數為NA | |
| B. | 在18g18O2中含有NA個18O原子 | |
| C. | 0.10mol Fe粉與足量水蒸氣反應轉移的電子數為0.30 NA | |
| D. | 將0.1mol硅酸鈉溶于1L水中,所得溶液中含有0.2NA個Na+ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
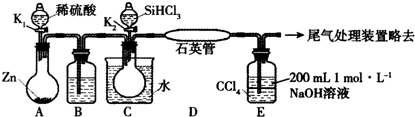
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
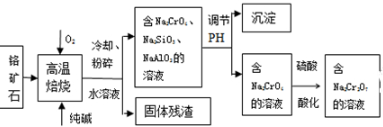
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol NaCl 分子 | |
| B. | 質子數為 35、中子數為 45 的溴原子:${\;}_{35}^{45}$ Br | |
| C. | 硫離子的結構示意圖: | |
| D. | NH4+ 的電子式: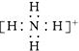 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
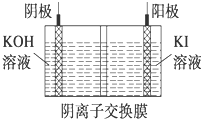 碘被稱為“智力元素”,科學合理地補充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘鹽中.
碘被稱為“智力元素”,科學合理地補充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘鹽中.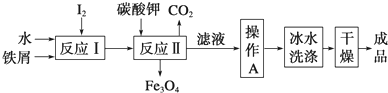
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com