
| A. | 3p軌道上有2個未成對電子的原子和4p軌道上有2個未成對電子的原子 | |
| B. | 3p軌道上只有1個空軌道的原子和4p軌道上只有1個空軌道的原子 | |
| C. | 最外層電子排布為1s2的原子和最外層電子排布為2s2的原子 | |
| D. | 最外層電子排布為3s2的原子和最外層電子排布為4s2的原子 |
分析 A.p軌道上有2個未成對電子,可能為2或4;
B.p軌道上只有1個空軌道,應含有2個電子;
C.最外層電子排布為1s2的為He,最外層電子排布為2s22p2的原子為C;
D.最外層電子排布為4s2的原子有Ca、V、Mn、Co、Ni、Zn等元素.
解答 解:A.p軌道上有2個未成對電子,可能為2或4,不能確定元素的種類,則不一定為同一主族,故A錯誤;
B.p軌道上只有1個空軌道,應含有2個電子,應為ⅣA族元素,故B正確;
C.最外層電子排布為1s2的為He,最外層電子排布為2s22p2的原子為C,故C錯誤;
D.最外層電子排布為3s2的原為Mg,最外層電子排布為4s2的原子有Ca、V、Mn、Co、Ni、Zn等元素,故D錯誤.
故選B.
點評 本題考查原子的結構與元素周期表的關系,題目難度不大,注意把握原子核外電子的排布特點,注意相關基礎知識的積累,試題培養了學生的分析能力及邏輯推理能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
 ,其中-R為烴基.
,其中-R為烴基.
 ;C的結構簡式
;C的結構簡式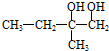 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
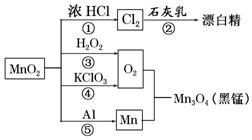
| A. | 只有反應①②④屬于氧化還原反應 | |
| B. | 反應⑤說明該條件下鋁可用于制熔點較高的金屬 | |
| C. | 相同條件下生成等量的O2,反應③和④轉移的電子數之比為1:1 | |
| D. | 反應①中氧化劑與還原劑的物質的量之比為1:4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖把氣體緩慢通過盛有足量試劑的試劑瓶A,在試管B中可以觀察到明顯現象的是( )
如圖把氣體緩慢通過盛有足量試劑的試劑瓶A,在試管B中可以觀察到明顯現象的是( )| 選項 | 氣體 | A中試劑 | B中試劑 |
| A | SO2、CO2 | 酸性KMnO4溶液 | 品紅溶液 |
| B | Cl2、HCl | 濃硫酸 | KI淀粉溶液 |
| C | NH3、CO2 | 濃硫酸 | 酚酞試液 |
| D | C2H4、CH4 | 酸性KMnO4溶液 | 溴的CCl4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
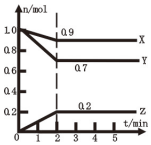 (1)某溫度時,在2L容器中X、Y、Z三種氣體物質的物質的量(n)隨著時間(t)變化的曲線如圖所示.
(1)某溫度時,在2L容器中X、Y、Z三種氣體物質的物質的量(n)隨著時間(t)變化的曲線如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 氯及其化合物在生產、生活中有廣泛的用途.回答下列問題:
氯及其化合物在生產、生活中有廣泛的用途.回答下列問題:| 容器編號 | 溫度/ | 容器體積/L | ClO2(g)的平衡轉化率 |
| a | T1 | V1=1L | 75% |
| b | T2 | V2 | |
| c | T3 | V3 | 75% |
| d | |||
| e |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 壓強 溫度 | 1×105Pa | 5×105Pa | 10×105Pa | 50×105Pa | 100×105Pa |
| 450℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 500℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com