

分析 (1)8CuFeS2+21O2 $\frac{\underline{\;高溫\;}}{\;}$ 8Cu+4FeO+2Fe2O3+16SO2中,Cu元素的化合價由+2價降低為0、O元素的化合價由0降低為-2價,Fe元素的化合價由+2價升高為+3價、S元素的化合價由-2價升高為+4價;
(2)鐵離子遇KSCN溶液為血紅色;
(3)二氧化硫為環境污染物,不能排放,可用于制備硫酸或亞硫酸鹽;
(4)二氧化硫具有漂白性,且漂白具有暫時性;
(5)實驗室制備,收集干燥的SO2,由裝置可知,A為反應裝置,C為干燥裝置,B為收集裝置,D為防止倒吸,E為尾氣處理,以此來解答.
解答 解:(1)8CuFeS2+21O2 $\frac{\underline{\;高溫\;}}{\;}$ 8Cu+4FeO+2Fe2O3+16SO2中,Cu元素的化合價由+2價降低為0、O元素的化合價由0降低為-2價,反應中被還原的元素是Cu、O,
故答案為:Cu、O;
(2)用稀H2SO4浸泡上述反應制取銅后剩余的固體殘渣,取少量所得溶液,檢驗溶液中存在Fe3+的方法是取少量溶液,滴加KSCN溶液,溶液變紅,
故答案為:取少量溶液,滴加KSCN溶液,溶液變紅;
(3)二氧化硫為環境污染物,不能高空排放,與濃硫酸不反應,可用于制備硫酸或亞硫酸鹽,只有bc符合,故答案為:bc;
(4)驗證黃銅礦冶煉銅的反應后氣體中含有SO2的方法是將氣體通入品紅溶液中,如果品紅溶液褪色,加熱后又變紅,則證明有SO2,
故答案為:將氣體通入品紅溶液中,如果品紅溶液褪色,加熱后又變紅,則證明有SO2;
(5)①裝置A產生SO2,反應的化學方程式為Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O,
故答案氣味:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O;
②由裝置可知,A為反應裝置,C為干燥裝置,B為收集裝置,D為防止倒吸,E為尾氣處理,則按氣流方向連接各儀器接口,順序為a→d→e→c→f,裝置D的作用是 安全瓶,防止倒吸;裝置E中NaOH溶液的作用是吸收多余的SO2,防止污染空氣,
故答案為:d;e;c;b;安全瓶,防止倒吸;吸收多余的SO2,防止污染空氣.
點評 本題考查物質的制備實驗,為高頻考點,把握制備原理、實驗裝置、實驗技能為解答的關鍵,側重分析與實驗力的考查,注意二氧化硫的性質及環境保護,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 清晨的陽光穿過茂密的林木枝葉所產生的美麗景象(美麗的光線) | |
| B. | 尿毒癥患者使用血液透析治療 | |
| C. | 明礬凈水 | |
| D. | 向FeCl3溶液中加入NaOH溶液,會出現紅褐色 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| H2CO3 | H2SO3 | HNO2 | HClO |
| K1=4.4×10-7 K2=4.7×10-11 | K1=1.2×10-2 K2=6.6×10-8 | K=7.2×10-4 | K=2.9×10-8 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
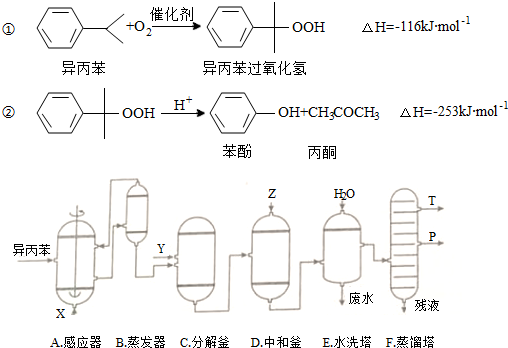
| 物質 | 相對分子質量 | 密度(g/cm-3) | 沸點/℃ |
| 異丙苯 | 120 | 0.8640 | 153 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 苯酚 | 94 | 1.0722 | 182 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

| 密度(g•cm-3) | 熔點(℃) | 沸點(℃) | 溶解性 | |
| 環己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 環己烯 | 0.81 | -103 | 83 | 難溶于水 |
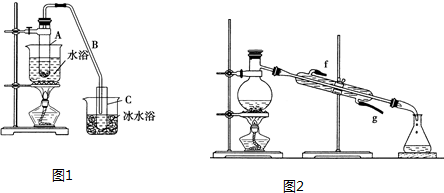
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 成 分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶于酸的物質 |
| 質量分數/% | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
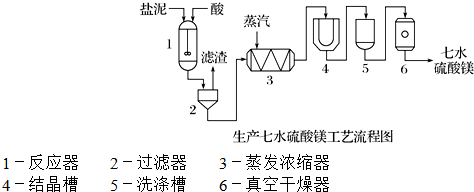
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaHSO3溶液與NaOH溶液反應:HSO3-+OH-═SO32-+H2O | |
| B. | 少量二氧化碳通入足量的NaOH溶液:CO2+2OH-═CO32-+H2O | |
| C. | Ba(OH)2與H2SO4反應:H++OH-═H2O | |
| D. | 氨水和醋酸溶液混合:NH3•H2O+CH3COOH═NH4++CH3COO-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將鐵粉加入稀硫酸中:Fe+2H+═Fe2++H2↑ | |
| B. | NaHCO3溶液中加入HCl:CO32-+2H+═CO2↑+H2O | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | MnO2與濃鹽酸反應制Cl2:MnO2+4HCl═Mn2++2Cl-+Cl2↑+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 鋁電池性能優越,Al-AgO電池可用作水下動力電源,其原理如圖所示.該電池反應的化學方程式為2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O.
鋁電池性能優越,Al-AgO電池可用作水下動力電源,其原理如圖所示.該電池反應的化學方程式為2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com