
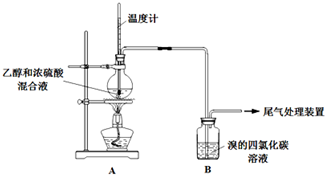
| 操 作 | 現 象 |
| 點燃酒精燈,加熱至170℃ | Ⅰ:A中燒瓶內液體漸漸變黑 Ⅱ:B內氣泡連續冒出,溶液逐漸褪色 |
| … | |
| 實驗完畢,清洗燒瓶 | Ⅲ:A中燒瓶內附著少量黑色顆粒狀物,有刺激性氣味逸出 |

分析 (1)濃硫酸具有脫水性、吸水性和強氧化性,能使乙醇碳化;
(2)①乙烯可與溴水發生加成反應;
②溴單質可以和二氧化硫發生氧化還原反應;
③a、氫氧化鈉可以和二氧化硫發生反應;濃硫酸具有吸水性,可以做干燥劑;根據乙的設計,即要證明干燥的二氧化硫不能使溴的四氯化碳褪色,但能使品紅褪色,據此確定裝置連接順序;
b、二氧化硫使品紅褪色,受熱時又恢復紅色,根據這一性質判斷是否為二氧化硫使品紅褪色;
c、溴單質可以和二氧化硫發生氧化還原反應,硫酸根離子和鋇離子反應會生成白色沉淀;
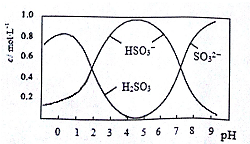
(3)根據圖可知,pH=4.5時,溶液中主要以亞硫酸氫根離子形式存在,據此書寫水解方程式;
(4)根據Ksp[BaSO4]=c(Ba2+)•c(SO42-),可計算出需要放熱c(Ba2+),進而計算最大濃度c(SO32-),據此答題;
解答 解:(1)濃硫酸具有脫水性,能使乙醇溶液“漸漸變黑”,故答案為:脫水;
(2)①根據甲的觀點,溴水可以使B中溶液褪色,反應的化學方程式是CH2=CH2+Br2→CH2Br-CH2Br,
故答案為:CH2=CH2+Br2→CH2Br-CH2Br;
②乙根據現象Ⅲ認為產生了SO2和水,在B中溴單質可以和二氧化硫、水發生氧化還原反應生存溴化氫和硫酸,
故答案為:H2O;
③a、根據甲的設計,洗氣瓶中盛放的試劑是氫氧化鈉,可以和二氧化硫反應,吸收二氧化硫,排除二氧化硫的干擾,根據乙的設計,C中盛放的試劑是,濃硫酸具有吸水性,可以做干燥劑,根據乙的設計,即要證明干燥的二氧化硫不能使溴的四氯化碳褪色,但能使品紅褪色,所以裝置連接順序為(d)cabe(f),
故答案為:NaOH 溶液;濃硫酸;(d)cabe(f);
b、證明SO2使E中溶液褪色的實驗是加熱已經褪色的品紅溶液,若紅色恢復,證明是SO2使品紅溶液褪色而不是Br2,
故答案為:加熱已經褪色的品紅溶液,若紅色恢復,證明是SO2使品紅溶液褪色而不是Br2;
c、溴單質可以和二氧化硫發生氧化還原反應,生成硫酸根離子和溴離子,硫酸根離子和鋇離子反應會生成白色沉淀,相關反應的離子方程式為SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓,
故答案為:SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓;
(3)根據圖可知,pH=4.5時,溶液中主要以亞硫酸氫根離子形式存在,所以水解方程式為Na2S2O5+H2O=2NaHSO3,
故答案為:Na2S2O5+H2O=2NaHSO3;
(4)根據Ksp[BaSO4]=c(Ba2+)•c(SO42-),可知需要c(Ba2+)=$\frac{Ksp(BaS{O}_{4})}{c(S{O}_{4}^{2-})}$=$\frac{1×1{0}^{-10}}{1×1{0}^{-5}}$=10-5mol•L-1,則溶液中SO32-的最大濃度c(SO32-)=$\frac{Ksp(BaS{O}_{3})}{c(B{a}^{2+})}$=$\frac{5×1{0}^{-7}}{1{0}^{-5}}$=0.05mol•L-1,
故答案為:0.05.
點評 本題考查學生乙醇的化學性質、圖象分析、離子濃度的計算等,結合實驗考查增加了題目的難度,綜合性較強,要求學生具有分析和解決問題的能力.


科目:高中化學 來源: 題型:選擇題
| A. | 二氧化碳:K+、Na+、SiO32-、Cl- | B. | 氨氣:Ag+、Al3+、Na+、NO3- | ||
| C. | 氯化氫:Ca2+、Fe3+、NO3-、Cl- | D. | 氯氣:Na+、Ba2+、I-、HSO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
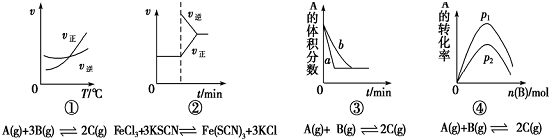
| A. | 圖①是其他條件一定時反應速率隨溫度變化的圖象,圖象表明,較低溫度下升溫平衡逆向移動,較高溫度下升溫平衡正向移 | |
| B. | 圖②是在平衡體系的溶液中加入少量KCl晶體后化學反應速率隨時間的變化 | |
| C. | 圖③可能是催化劑對化學平衡的影響,也可能是其它因素對化學平衡的影響 | |
| D. | 圖④是一定條件下,向含有一定量A的容器中逐漸加入B時的圖象,壓強p1>p2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
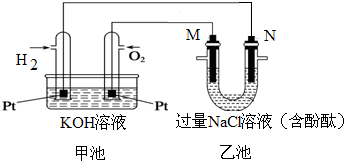 如圖所示是氫氧燃料電池工作時的裝置,乙池中的兩個電極均是石墨電極,請回答下列問題:
如圖所示是氫氧燃料電池工作時的裝置,乙池中的兩個電極均是石墨電極,請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 括號內為雜項 | 除雜試劑 | 除雜操作 | |
| A | Na2O2(Na2O) | O2 | 在純氧中加熱 |
| B | Na2CO3(NaHCO3) | CO2 | 通入過量的CO2 |
| C | FeCl(FeCl2) | Cl2 | 通入過量的Cl2 |
| D | FeSO4(CuSO4) | Fe | 加入過量的Fe粉,充分反應后過濾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 制備AlCl3、FeCl3、CuCl2均不能采用將溶液直接蒸干的方法 | |
| B. | 在鍍件上電鍍鋅,用鋅作陽極 | |
| C. | 用如圖1裝置生產家用消毒液(NaClO) | |
| D. | 用如圖2裝置為鉛蓄電池充 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常數K | 10 | 9 | 1 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
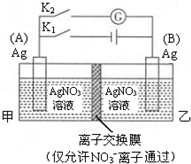
| A. | 閉合K1,斷開K2后,A電極增重 | |
| B. | 閉合K1,斷開K2后,乙池溶液中Ag+濃度增大 | |
| C. | 斷開K1,閉合K2后,B電極發生氧化反應 | |
| D. | 斷開K1,閉合K2后,NO3-向A電極移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電器起火,立即用水撲滅 | |
| B. | 炒菜時油鍋著火,立即蓋上鍋蓋 | |
| C. | 廚房煤氣管道漏氣,立即關閉閥門并開窗通風 | |
| D. | 圖書管內圖書著火,立即用液態二氧化碳滅火器撲滅 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com