
 (1)拆開1mol H-H鍵,1mol N-H鍵,1mol N三N鍵分別需要吸收的能量為436kJ,391kJ,946kJ,則理論上,每生成1mol NH3放出(填:吸收或放出)熱量46 kJ;
(1)拆開1mol H-H鍵,1mol N-H鍵,1mol N三N鍵分別需要吸收的能量為436kJ,391kJ,946kJ,則理論上,每生成1mol NH3放出(填:吸收或放出)熱量46 kJ;分析 (1)化學反應中,化學鍵斷裂吸收能量,形成新化學鍵放出能量,根據方程式計算,化學反應中,反應物的總能量大于生成物的總能量,反應放熱,反之吸熱,以此計算反應熱并判斷吸熱還是放熱;
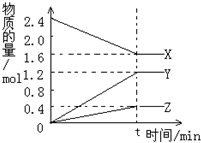
(2)①由圖象可以看出,反應中X的物質的量減小,Y、Z的物質的量增多,則X為反應物,Y、Z為生成物.t時刻后,X的物質的量為定值且不為零,為可逆反應,且△n(X):△n(Y):△n(Z)=(2.4mol-1.6mol):1.2mol:0.4mol=0.8mol:1.2mol:0.4mol=2:3:1,得到反應的化學方程式;
②在tmin時間內,用Y表示反應的平均速率v(Y)=$\frac{△c}{△t}$;
③X、Y、Z各物質的量不再隨時間的變化而變化,說明達到平衡狀態.
解答 解:(1)拆1molH-H鍵、1molN≡N、1molN-H鍵分別需要吸收的能量為436kJ、946kJ、391kJ,在反應N2+3H2?2NH3中,斷裂3mol H-H鍵,1mol N三N鍵共吸收的能量為:3×436kJ+946kJ=2254kJ,
生成2mol NH3,共形成6molN-H鍵,放出的能量為:6×391kJ=2346kJ,
吸收的能量少,放出的能量多,該反應為放熱反應,
放出的熱量為:2346kJ-2254kJ=92kJ,
所以生成1mol NH3放出熱量為46KJ;
故答案為:放出;46;
(2)①由圖象可以看出,反應中X的物質的量減小,Y、Z的物質的量增多,則X為反應物,Y、Z為生成物.t時刻后,X的物質的量為定值且不為零,為可逆反應,且△n(X):△n(Y):△n(Z)=(2.4mol-1.6mol):1.2mol:0.4mol=0.8mol:1.2mol:0.4mol=2:3:1,物質在反應中物質的量之比等于化學方程式計量數之比,則反應的化學方程式為:2X?3Y+Z;
故答案為:2X?3Y+Z;
②在tmin時間內,用Y表示反應的平均速率v(Y)=$\frac{△c}{△t}$=$\frac{\frac{1.2mol}{2L}}{3min}$=0.2mol/(L﹒min),故答案為:0.2mol/(L﹒min);
③X、Y、Z各物質的量不再隨時間的變化而變化,說明達到平衡狀態,故答案為:平衡.
點評 本題考查反應熱的計算,物質的量或濃度隨時間的變化曲線 化學反應速率變化曲線及其應用,涉及化學方程式、平衡狀態、反應速率的計算等問題,題目難度不大,注意相關知識的積累.


科目:高中化學 來源: 題型:解答題
| 溶液 | ①品紅溶液 | ②Na2S | ③BaCl2 | ④Ba(OH)2 | ⑤Ba(NO3)2 |
| 現象 | 溶液褪色 | 黃色沉淀 | 無明顯現象 | 白色沉淀 | 白色沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | B的最簡氣態氫化物的熱穩定性比A的強是因為其最簡氣態氫化物分子間存在氫鍵 | |
| B. | 由A元素構成的單質均具有熔點高、硬度大的特性 | |
| C. | 常溫下E與D元素形成的化合物1mol與水完全反應生成氣體的質量為2克 | |
| D. | 由A、B、C、D四種元素形成的化合物一定既有離子鍵,又有共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 瑞典皇家科學院2010年10月5日宣布,將2010年諾貝爾物理學獎授予荷蘭籍物理學家安德烈•海姆和擁有英國與俄羅斯雙重國籍的物理學家康斯坦丁•諾沃肖洛夫,以表彰他們在石墨烯材料方面的卓越研究.石墨烯結構如下圖.它不僅是已知材料中最薄的一種,還非常牢固堅硬;作為單質,它在室溫下傳遞電子的速度比已知導體都快.下列有關石墨烯的說法正確的是( )
瑞典皇家科學院2010年10月5日宣布,將2010年諾貝爾物理學獎授予荷蘭籍物理學家安德烈•海姆和擁有英國與俄羅斯雙重國籍的物理學家康斯坦丁•諾沃肖洛夫,以表彰他們在石墨烯材料方面的卓越研究.石墨烯結構如下圖.它不僅是已知材料中最薄的一種,還非常牢固堅硬;作為單質,它在室溫下傳遞電子的速度比已知導體都快.下列有關石墨烯的說法正確的是( )| A. | 石墨烯和石墨燃燒都生成二氧化碳,說明它們互為同分異構體 | |
| B. | 石墨烯一定條件下可與氫氣發生反應生成石墨烷 | |
| C. | 石墨烯在室溫下傳遞電子的速度快是因為碳原子間以極性鍵結合 | |
| D. | 12g石墨烯中含有NA個六元碳環 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 科學家們正在研究利用藍綠藻等低等植物和微生物在陽光作用下使水分解產生氫氣 | |
| B. | 貯氫金屬在一定溫度和壓強下可以吸附氫氣,如鑭鎳合金(LaNi5)可以吸附氫氣形成LaNi5H6,其中H元素仍以H2分子形式存在 | |
| C. | 氫氣因具有高熱值、燃燒產物無污染等優點而被看成是理想的綠色能源 | |
| D. | 燃燒樹枝取熱、將植物秸桿制沼氣、用淀粉制乙醇都是人們利用生物質能的方式 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com