
| A. | 在上述兩個反應中,當有1molP參加反應時,反應轉移電子數(shù)均為5NA | |
| B. | 在反應(2)中,當生成3mol硫酸時,被還原的P為1mol | |
| C. | 在上述兩個反應中,P均作還原劑 | |
| D. | 在上述兩個反應中,還原產(chǎn)物都是H3PO4 |
分析 2P+5CuSO4+8H2O═5Cu+2H3PO4+5H2SO4該反應中P元素化合價由0價變?yōu)?價,Cu元素化合價由+2價變?yōu)?價;
11P+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4該反應中P元素化合價由0價變?yōu)?3價、+5價,Cu元素化合價由+2價變?yōu)?1價,如果有11molP參加氧化還原反應,則有$\frac{6}{11}$的P被氧化,其余的P被還原,據(jù)此分析解答.
解答 解:2P+5CuSO4+8H2O═5Cu+2H3PO4+5H2SO4該反應中P元素化合價由0價變?yōu)?價,Cu元素化合價由+2價變?yōu)?價;
11P+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4該反應中P元素化合價由0價變?yōu)?3價、+5價,Cu元素化合價由+2價變?yōu)?1價,如果有11molP參加氧化還原反應,則有$\frac{6}{11}$的P被氧化,其余的P被還原,
A.在反應(2)中,11molP參加氧化還原反應,則有$\frac{6}{11}$的P被氧化,則當有1molP參加反應時,被氧化的P為$\frac{6}{11}$mol,轉移電子為$\frac{6}{11}$mol×5,反應轉移電子數(shù)為$\frac{30}{11}$NA,故A錯誤;
B.在反應(2)中,生成15molH2SO4,被還原的P為$\frac{5}{11}$×11mol=5mol,則當生成3mol硫酸時,被還原的P為1mol,故B正確;
C.在反應(2)中,P元素化合價由0價變?yōu)?3價、+5價,所以P既是氧化劑又是還原劑,故C錯誤;
D.在反應(1)中,P元素被氧化,H3PO4是氧化產(chǎn)物,故D錯誤;
故選B.
點評 本題考查氧化還原反應,明確元素化合價變化是解本題關鍵,注意該反應中P元素化合價變化,為易錯點,側重于考查學生對基礎知識的應用能力.


科目:高中化學 來源: 題型:選擇題
| A. | 高溫、高壓 | B. | 適宜的溫度、高壓、催化劑 | ||
| C. | 低溫、低壓 | D. | 高溫、高壓、催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
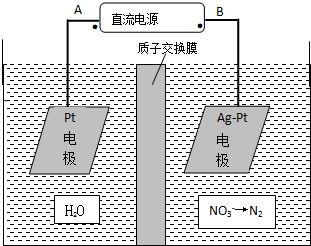 硝酸是一種重要的化工原料,工業(yè)上一般以氨氣為原料來制備硝酸.請回答:
硝酸是一種重要的化工原料,工業(yè)上一般以氨氣為原料來制備硝酸.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
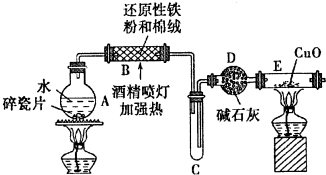
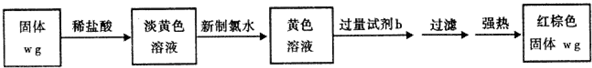
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
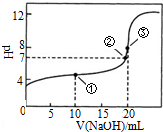 常溫下,用0.1000mol•L-1NaOH溶液滴定 20.00mL1000mol•L-1CH3COOH溶液滴定曲線如圖.下說法正確的是( )
常溫下,用0.1000mol•L-1NaOH溶液滴定 20.00mL1000mol•L-1CH3COOH溶液滴定曲線如圖.下說法正確的是( )| A. | 滴定過程中可能出現(xiàn):c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | |
| B. | 點①所示溶液中:c(CH3COOH)+c(CH3COO-)>2c(Na+) | |
| C. | 點③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 點③所示溶液中:c(CH3COO-)>c(Na+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不慎將酸濺到眼中,應立即用水沖洗,邊洗邊眨眼睛 | |
| B. | 不慎將濃堿溶液沾到皮膚上,要立即用大量水沖洗,然后涂上硼酸溶液 | |
| C. | 配制硫酸溶液時,可先在量筒中加入一定體積的水,再在攪拌下加入濃硫酸 | |
| D. | 上述說法均不正確 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 A、B、C、D、E五種常見元素的核電荷數(shù)依次增大.A的基態(tài)原子中有2個未成對電子,B是地殼中含量最多的元素,C是短周期中最活潑的金屬元素,D與C可形成CD型離子化合物,E的基態(tài)3d軌道上有2個電子.請回答下列問題:
A、B、C、D、E五種常見元素的核電荷數(shù)依次增大.A的基態(tài)原子中有2個未成對電子,B是地殼中含量最多的元素,C是短周期中最活潑的金屬元素,D與C可形成CD型離子化合物,E的基態(tài)3d軌道上有2個電子.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
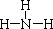 ,寫出甲與足量的氫氧化鈉溶液反應的化學方程式為AlN+NaOH+H2O=NaAlO2+NH3↑,驗證溶液丁中產(chǎn)物陰離子的實驗方法為取少量溶液丁于試管中,逐滴加入稀鹽酸,若先產(chǎn)生白色沉淀后消失,說明為NaAlO2.
,寫出甲與足量的氫氧化鈉溶液反應的化學方程式為AlN+NaOH+H2O=NaAlO2+NH3↑,驗證溶液丁中產(chǎn)物陰離子的實驗方法為取少量溶液丁于試管中,逐滴加入稀鹽酸,若先產(chǎn)生白色沉淀后消失,說明為NaAlO2.查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com