
| A. | -16Q kJ/mol | B. | +8Q kJ/mol | C. | +16 Q kJ/mol | D. | -8 Q kJ/mol |
分析 充分燃燒一定量的丁烷發生的反應為:2C4H10+13O2$\frac{\underline{\;點燃\;}}{\;}$8CO2+10H2O,CO2恰好與KOH溶液完全反應生成正鹽為K2CO3,2KOH+CO2═K2CO3+H2O,根據n=c×V計算KOH的物質的量,根據鉀元素守恒計算n(K2CO3),根據碳元素守恒有n(CO2)=n(K2CO3),據此計算判斷.
解答 解:KOH的物質的量為n(KOH)=c×V=0.2L×5mol/L=1mol,
2KOH+CO2═K2CO3+H2O,
根據鉀離子守恒,故n(K2CO3)=mol×$\frac{1}{2}$=0.5mol,
根據碳元素守恒由n(CO2)=n(K2CO3)=0.5mol,
2C4H10+13O2$\frac{\underline{\;點燃\;}}{\;}$8CO2+10H2O
根據碳元素守恒可知,丁烷的物質的量為n(C4H10)=0.5mol×$\frac{1}{4}$=$\frac{1}{8}$mol,
即$\frac{1}{8}$mol丁烷放出的熱量大小為QkJ,
故1mol丁烷完全燃燒放出的熱量為QkJ×8=8QkJ,
則此條件下反應熱化學方程式為C4H10(g)+$\frac{13}{2}$O2(g)═4CO2(g)+5H2O(l)△H=-8Q kJ•mol-1,
故選D.
點評 本題考查反應熱的計算,根據氫氧化鉀確定丁烷的物質的量是解答該題的關鍵,題目難度中等.


科目:高中化學 來源: 題型:解答題
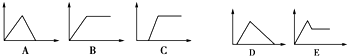 在圖中,橫坐標為向一定量的某溶液中加入某物質的量,縱坐標為生成沉淀的量.從圖A~E中,選擇適合表中各題要求的序號填入表中.
在圖中,橫坐標為向一定量的某溶液中加入某物質的量,縱坐標為生成沉淀的量.從圖A~E中,選擇適合表中各題要求的序號填入表中.| 溶液 | 加(通)入物質 | 序號 |
| (1)飽和石灰水 | 通入過量CO2 | |
| (2)AlCl3溶液 | 加入過量的NH3•H2O | |
| (3)含少量NaOH的Na[Al(OH)4]溶液 | 通入過量CO2 | |
| (4)含少量NaOH的Na[Al(OH)4]溶液 | 逐滴加入稀鹽酸 | |
| (5)MgCl2、AlCl3混合液 | 逐滴加入NaOH溶液至過量 | |
| (6)NaOH溶液 | 逐滴加入AlCl3溶液至過量 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) | B. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) | ||
| C. | c(Cl-)=c(NH4+)>c(H+)=c(OH-) | D. | c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2SO4 | B. | KCl | C. | NaOH | D. | CuSO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 已達平衡狀 | B. | 未達平衡狀態,反應正向進行 | ||
| C. | 未達平衡狀態,反應逆向進行 | D. | 無法確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 離子半徑:c>b>a | |
| B. | a與c形成化合物的溶液有毒,要密封保存于玻璃瓶中 | |
| C. | a2b2與d的一種較高價態離子的鹽溶液混合時會產生大量的b2 | |
| D. | d高價離子在溶液中與c的低價離子因發生氧化還原反應而不能大量共存 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com