
| A. | 沸點:Br2>Cl2 | B. | 穩定性:HCl>HBr | ||
| C. | 酸性:H2SiO3>H2SO4 | D. | 堿性:Mg(OH)2<NaOH |
分析 A.分子晶體熔沸點與其相對分子質量成正比;
B.元素的非金屬性越強,其氫化物的穩定性越強;
C.元素的非金屬性越強,其最高價氧化物的水化物酸性越強;
D.元素的金屬性越強,其最高價氧化物的水化物堿性越強.
解答 解:A.分子晶體熔沸點與其相對分子質量成正比,溴和氯氣都是分子晶體,相對分子質量溴大于氯氣,所以沸點Br2>Cl2,故A正確;
B.元素的非金屬性越強,其氫化物的穩定性越強,非金屬性Cl>Br,所以穩定性:HCl>HBr,故B正確;
C.元素的非金屬性越強,其最高價氧化物的水化物酸性越強,非金屬性S>Si,所以酸性:H2SiO3<H2SO4,故C錯誤;
D.元素的金屬性越強,其最高價氧化物的水化物堿性越強,金屬性Mg<Na,所以堿性Mg(OH)2<NaOH,故D正確;
故選C.
點評 本題考查同一周期同一主族元素周期律,為高頻考點,明確金屬性、非金屬性強弱判斷是解本題關鍵,注意分子晶體熔沸點與分子間作用力有關,與化學鍵無關,易錯選項是A.


 藍天教育暑假優化學習系列答案
藍天教育暑假優化學習系列答案科目:高中化學 來源: 題型:選擇題
| A. | 23 g Na與足量H2O反應完全后可生成NA個H2分子 | |
| B. | 1 mol Na2O2和足量CO2反應轉移2 NA個電子 | |
| C. | 標準狀況下,22.4 L N2和H2混合氣中含NA個原子 | |
| D. | 3 mol單質Fe完全轉變為Fe3O4,失去8 NA個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2H4+O2═N2+2H2O△H=-534.4 kJ•mol-1 | |
| B. | N2H4+O2═N2+2H2O△H=-1 068.8 kJ•mol-1 | |
| C. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.4 kJ•mol-1 | |
| D. | $\frac{1}{2}$N2H4(g)+$\frac{1}{2}$O2(g)═$\frac{1}{2}$N2(g)+H2O(g)△H=+267.2 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 48gO3含有的氧原子數目為NA | |
| B. | 常溫常壓下,22.4L Cl2含有的分子數目為NA | |
| C. | 1molAl與足量氫氧化鈉溶液完全反應時失去的電子數目為3NA | |
| D. | 1mol•L-1K2CO3溶液中含有的鉀離子數目為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
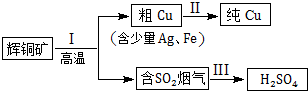
| 所含離子 | Na+ | HCO3- | CO32- | SO32- | HSO3- |
| 濃度mol/L | 0.005 | 0.01 | 0.05 | 0.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
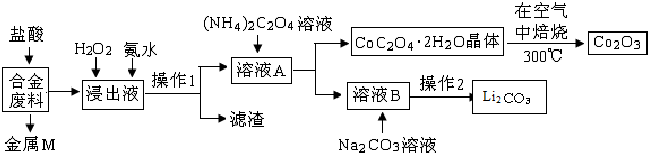
| 溫度/℃ | 10 | 30 | 60 | 90 |
| 濃度/mol?L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
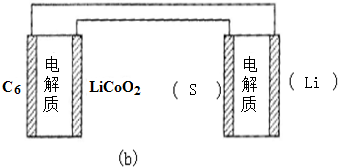 中填寫“Li”或“S”,以達到給鋰硫電池充電的目的.
中填寫“Li”或“S”,以達到給鋰硫電池充電的目的.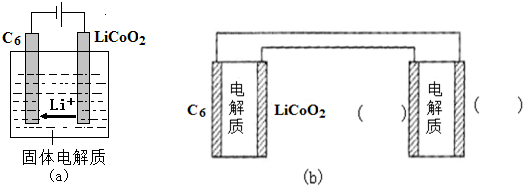
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硫溶于水能導電,故二氧化硫屬于電解質 | |
| B. | 硫酸鋇難溶于水,故硫酸鋇屬于弱電解質 | |
| C. | 硫酸是強電解質,故純硫酸能導電 | |
| D. | 氫氧根離子濃度相同的氫氧化鈉溶液和氨水導電能力相同 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com