
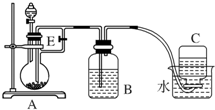
 如圖所示裝置可用來制取Fe(OH)2和觀察Fe(OH)2在空氣中被氧化時的顏色變化.實驗提供的試劑:鐵屑、6mol/L硫酸溶液、NaOH溶液.下列說法錯誤的是( )
如圖所示裝置可用來制取Fe(OH)2和觀察Fe(OH)2在空氣中被氧化時的顏色變化.實驗提供的試劑:鐵屑、6mol/L硫酸溶液、NaOH溶液.下列說法錯誤的是( )| A. | B中盛有一定量的NaOH溶液,A中應預先加入的試劑是鐵屑 | |
| B. | 實驗開始時應先將活塞E關閉 | |
| C. | 生成Fe(OH)2的操作為:關閉E,使A中溶液壓入B瓶中 | |
| D. | 取下裝置B中的橡皮塞,使空氣進入,有關反應的化學方程式為:4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
分析 A、制取硫酸亞鐵需要鐵屑,所以在燒瓶中應該先加入鐵屑;
B、鐵和稀硫酸反應生成硫酸亞鐵和氫氣,該反應中有氣體生成,應先將活塞E打開;
C、關閉活塞E,利用氣體壓強使FeSO4溶液被壓入B瓶中進行反應;
D、氫氧化亞鐵不穩定,容易被空氣中的氧氣氧化生成氫氧化鐵.
解答 解:A、制取硫酸亞鐵需要鐵屑,所以在燒瓶中應該先加入鐵屑,所以A中應預先加入的試劑是鐵屑,故A正確;
B、稀硫酸和鐵反應生成硫酸亞鐵和氫氣,因為有氣體生成,如果不打開活塞E,會造成安全事故,所以要打開活塞E,故B錯誤;
C、鐵和硫酸反應有氫氣生成,關閉活塞E,導致A裝置中氫氣所產生的壓強逐漸增大使FeSO4溶液被壓入B瓶中進行反應生成氫氧化亞鐵,所以操作為:關閉活塞E,使FeSO4溶液被壓入B瓶中進行反應,故C正確;
D、氫氧化亞鐵不穩定,容易被空氣中的氧氣氧化生成紅褐色的氫氧化鐵,反應方程式為:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故D正確;
故選B.
點評 本題考查了氫氧化亞鐵的制取,難度不大,氫氧化亞鐵極易被氧氣氧氣,所以制取氫氧化亞鐵時注意必須在無氧氣的條件下進行反應,這是高中化學中較重要的一個實驗,是學習的重點.


科目:高中化學 來源: 題型:選擇題
| A. | 用惰性電極電解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 向NaClO溶液中滴加少量FeSO4溶液:5ClO-+2Fe2++5H2O═4HClO+Cl-+2Fe(OH)3↓ | |
| C. | 向NH4HCO3稀溶液中滴加過量Ca(OH)2溶液:NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O | |
| D. | 向CuSO4溶液中滴加過量氨水:Cu2++2 NH3•H2O═Cu(OH)2↓+2 NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
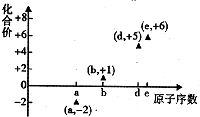 如圖是邵分短周期元素的原子序數與其某種常見化合價的關系圖,若用原子序數代表所對應的元素,則下列說法正確的是( )
如圖是邵分短周期元素的原子序數與其某種常見化合價的關系圖,若用原子序數代表所對應的元素,則下列說法正確的是( )| A. | 31d和33d屬于同種核素 | B. | 第一電離能d>e,電負性d<e | ||
| C. | 氣態氫化物的穩定性:a>d>e | D. | a和b形成的化合物不可能含共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | C | CO | C2H6 | C2H5OH |
| 燃燒熱/KJ•mol-1 | 393.5 | 283 | 1559.8 | 1366.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶解、蒸發 | B. | 萃取、蒸餾 | C. | 分液、蒸餾 | D. | 萃取、過濾 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.3mol | B. | 0.4mol | C. | 0.5mol | D. | 0.6mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | 室溫下,試管中所加試劑及其用量/mL | 室溫下溶液顏色褪至無色所需時間/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 2.0 | 3.0 | 3.0 | 2.0 | 5.2 |
| 3 | 1.0 | 4.0 | 3.0 | 2.0 | 6.4 |
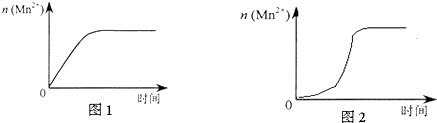
| 實驗編號 | 室溫下,試管中所加試劑及其用量/mL | 再向試管中加入少量固體 | 室溫下溶液顏色褪至無色所需時間/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 丙烷 | B. | 乙烷 | C. | 丙烯 | D. | 甲烷 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{r(Ca)}{r(Mg)}$ | B. | $\frac{r(C{l}^{-})}{r(A{l}^{3+})}$ | C. | $\frac{r(Na)}{r(Mg)}$ | D. | $\frac{r(N{a}^{+})}{r({F}^{-})}$ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com