
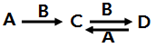 短周期主族元素X、Y、Z、W、M、N 的原子序數依次增大,且原子最外層電子數之和為23.X的原子半徑比Y的小,X與W同主族,Z的最外層電子數是電子層數的3倍,M是地殼中含量最高的金屬元素.
短周期主族元素X、Y、Z、W、M、N 的原子序數依次增大,且原子最外層電子數之和為23.X的原子半徑比Y的小,X與W同主族,Z的最外層電子數是電子層數的3倍,M是地殼中含量最高的金屬元素.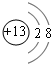 ,X、Y形成的含18電子的化合物為N2H4,電子式為
,X、Y形成的含18電子的化合物為N2H4,電子式為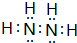 ,W、Z形成的只含離子鍵的化合物為Na2O,用電子式表示其形成過程為:
,W、Z形成的只含離子鍵的化合物為Na2O,用電子式表示其形成過程為: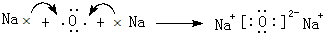 ,
, ;
;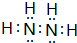 ;
;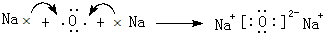 ;
; Al(OH)3+OH-,A與D反應的離子方程式為:Al3++3AlO2-+6H2O=4 Al(OH)3↓,
Al(OH)3+OH-,A與D反應的離子方程式為:Al3++3AlO2-+6H2O=4 Al(OH)3↓, Al(OH)3+OH-;Al3++3AlO2-+6H2O=4 Al(OH)3↓.
Al(OH)3+OH-;Al3++3AlO2-+6H2O=4 Al(OH)3↓.


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:
| A、用塊狀固體反應物代替粉末狀反應物 |
| B、提高設備抗壓強度以便加壓 |
| C、采用高溫高壓的反應條件 |
| D、選擇合適的催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
| 4 | ② | ④ |
查看答案和解析>>
科目:高中化學 來源: 題型:
 A、B兩種固體物質的溶解度曲線如圖所示.請回答:
A、B兩種固體物質的溶解度曲線如圖所示.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:
| A、pH=4 |
| B、[H+]=1×10-3mol?L-1 |
| C、[OH-]=1×10-12mol?L-1 |
| D、[OH-]=1×10-14mol?L-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com