
| A. | 平衡前,隨著反應的進行,容器內壓強始終不變 | |
| B. | 平衡時,分離出少量D,A的轉化率提高 | |
| C. | 平衡時,升高溫度,容器內混合氣體的密度減小 | |
| D. | 平衡時,充入C,該反應平衡常數減小 |
分析 將2mol A和1mol B充入到絕熱恒容密閉容器中,發生反應2A(g)+B(g)═3C(g)+D(s),達到平衡時測得容器內壓強增大,說明正反應是放熱反應,所以反應在恒溫恒容的密閉容器中進行,兩邊的氣體物質的量相等,所以容器內壓強始終不變,由此分析解答.
解答 解:A、兩邊的氣體物質的量相等,平衡前,隨著反應的進行,容器內壓強始終不變,故A正確;
B、D是固體,量變但濃度不變,平衡不移動,故B錯誤;
C、正反應是放熱反應,升高溫度平衡逆向移動,氣體質量增加,容器內混合氣體的密度增大,故C錯誤;
D、平衡常數是溫度的函數,溫度不變K不變,故D錯誤;
故選A.
點評 本題考查化學平衡移動,側重于學生的分析能力的考查,注意把握反應的特點,結合方程式以及影響因素解答該題,難度不大


 學練快車道快樂假期寒假作業系列答案
學練快車道快樂假期寒假作業系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.8mol/L | D. | 1mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在蒸餾水中加入大量NaOH固體,KW不變 | |
| B. | 0.1mol/LHF溶液的PH=2,則該溶液中c(OH-)>c(HF) | |
| C. | 在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-) | |
| D. | NaCl溶液和CH3COONH4溶液均顯中性,兩溶液中水的電離程度相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②④①③⑤ | B. | ④②①⑤③ | C. | ⑤③①④② | D. | ②④⑤①③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 往1.0mol•L-1KI溶液中加入固體I2,發生反應:I2(aq)+I- (aq)═I3-(aq)△H;I-的物質的量濃度c(I-)隨溫度T的變化曲線如圖所示.已知反應第一次達到平衡時用時10s,則下列說法正確的是( )
往1.0mol•L-1KI溶液中加入固體I2,發生反應:I2(aq)+I- (aq)═I3-(aq)△H;I-的物質的量濃度c(I-)隨溫度T的變化曲線如圖所示.已知反應第一次達到平衡時用時10s,則下列說法正確的是( )| A. | 該反應的△H>0 | |
| B. | a、c兩點對應的I-反應速率相等 | |
| C. | b點時0~10s I-的平均反應速率為0.04mol•L-1•s-1 | |
| D. | d點時該反應在對應溫度下處于平衡狀態 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
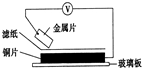
| A. | 若金屬片為鋅片,溶液為稀硫酸,則電子由銅片流向鋅片 | |
| B. | 若金屬片為鐵片,溶液為氯化鈉,則正極發生的電極反應為:O2+2H2O+4e-═4OH- | |
| C. | 若金屬片為鐵片,溶液為氯化鈉,為防止鐵片發生吸氧腐蝕,可以將銅片換成錫片 | |
| D. | 若濾紙浸有鹽溶液,金屬片分別用鋅片和鐵片接入,伏特表“示數”接入鋅片的大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | V≥$\frac{1}{18}$ | B. | V≤$\frac{1}{23}$ | C. | V<$\frac{1}{18}$ | D. | V≤$\frac{1}{56}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaOH的電子式: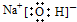 | |
| B. | 質子數和中子數均為16的硫原子:1616S | |
| C. | 氟原子的結構示意圖: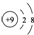 | |
| D. | 乙醛的結構簡式: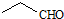 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com