
| A. | V≥$\frac{1}{18}$ | B. | V≤$\frac{1}{23}$ | C. | V<$\frac{1}{18}$ | D. | V≤$\frac{1}{56}$ |
分析 1g鈉、鋁、鐵的物質的量分別為$\frac{1}{23}$mol、$\frac{1}{27}$mol、$\frac{1}{56}$mol,由與硫酸的反應關系2Na~H2SO4、2Al~3H2SO4、Fe~H2SO4,可知,如完全反應,各需硫酸的物質的量為$\frac{1}{46}$mol、$\frac{1}{18}$mol、$\frac{1}{56}$mol,要使鋁、鐵反應后放出等量的氫氣,且比鈉反應生成的氫氣少,則說明與鐵、鋁反應時硫酸不足,而過量的鈉可與水反應,以此解答該題.
解答 解:要使鋁、鐵反應后放出等量的氫氣,且比鈉反應生成的氫氣少,則說明與鐵、鋁反應時硫酸不足,而過量的鈉可與水反應,
1g鈉、鋁、鐵的物質的量分別為$\frac{1}{23}$mol、$\frac{1}{27}$mol、$\frac{1}{56}$mol,由與硫酸的反應關系2Na~H2SO4、2Al~3H2SO4、Fe~H2SO4,可知,如完全反應,各需硫酸的物質的量為$\frac{1}{46}$mol、$\frac{1}{18}$mol、$\frac{1}{56}$mol,
則可知當硫酸的體積V≤$\frac{1}{56}$時,鐵、鋁過量,硫酸完全反應,生成的氫氣的物質的量≤$\frac{1}{56}$mol,
但過量的鈉可與水反應生成氫氣,1g鈉完全反應放出氫氣的物質的量為$\frac{1}{46}$mol,
故選D.
點評 本題考查過量問題的計算,側重于學生的分析能力和計算能力的考查,題目難度中等,根據要使鋁、鐵反應后放出等量的氫氣,且比鈉反應生成的氫氣少,則說明與鐵、鋁反應時硫酸不足是解題關鍵,注意掌握判斷反應物過量的計算題的解題方法與技巧.


科目:高中化學 來源: 題型:選擇題
| A. | 平衡前,隨著反應的進行,容器內壓強始終不變 | |
| B. | 平衡時,分離出少量D,A的轉化率提高 | |
| C. | 平衡時,升高溫度,容器內混合氣體的密度減小 | |
| D. | 平衡時,充入C,該反應平衡常數減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
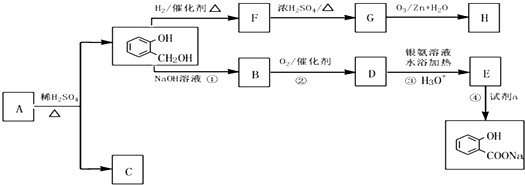
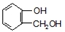 到F反應是否進行完全,可用FeCl3溶液檢驗
到F反應是否進行完全,可用FeCl3溶液檢驗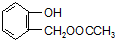 ,由F到G的反應類型為消去反應.
,由F到G的反應類型為消去反應.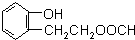 和
和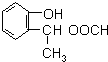 (不考慮立體異構).
(不考慮立體異構). .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,1mol21H2含有nA個質子 | |
| B. | 1molCu與足量FeCl3溶液充分反應轉移了2nA個電子 | |
| C. | 含49gH2SO4的硫酸溶液中含有nA個氫原子 | |
| D. | 標準狀況下,22.4L甲醇含有nA個分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
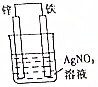 原電池原理的發現是儲能和功能技術的巨大進步,是化學對人類的一項重大貢獻.
原電池原理的發現是儲能和功能技術的巨大進步,是化學對人類的一項重大貢獻.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
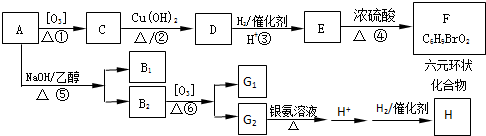
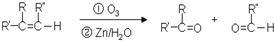
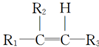 $\stackrel{[O_{3}]}{→}$
$\stackrel{[O_{3}]}{→}$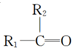 +
+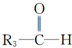
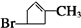

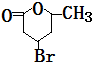 +H2O
+H2O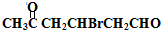 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$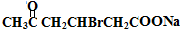 +Cu2O↓+3H2O
+Cu2O↓+3H2O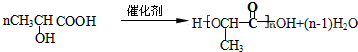
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
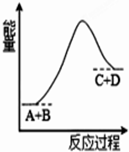
| A. | 該反應為釋放能量 | |
| B. | 該反應為吸收能量 | |
| C. | 反應物的總能量高于生成物的總能量 | |
| D. | 該反應只有在加熱條件下才能進行 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com