
| A. | NaCl | B. | LiCl | C. | MgO | D. | Na2S |
分析 離子化合物中,陰陽離子電子層結構相同,說明陽離子元素位于陰離子元素下一周期,且陰陽離子核外電子數相等,據此分析解答.
解答 解:A.NaCl中鈉離子核外有10個電子、Cl離子核外有18個電子,氯離子電子層比鈉離子多一個,電子層結構不同,故A錯誤;
B.LiCl中鈉鋰離子核外有2個電子、Cl離子核外有18個電子,氯離子電子層比鋰離子多2個,電子層結構不同,故B錯誤;
C.氧化鎂中氧離子和鎂離子核外電子數都是10,其陰陽離子電子層結構相同,故C正確;
D.Na2S中鈉離子核外有10個電子、硫離子核外有18個電子,硫離子比鈉離子多1個電子層,電子層結構不同,故D錯誤;
故選C.
點評 本題考查了原子結構和元素性質,明確原子核外電子排布及原子結構即可解答,電子層結構相同的離子中電子數相等,題目難度不大.


科目:高中化學 來源: 題型:解答題
 某同學設計了如圖的實驗裝置來粗略地測定電石中碳化鈣的質量分數.
某同學設計了如圖的實驗裝置來粗略地測定電石中碳化鈣的質量分數.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ( CH3)2CHCH2CH2CH3 | B. | (CH3CH2)2CHCH3 | C. | (CH3)2CHCH(CH3)2 | D. | (CH3)3CCH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 按系統命名法,化合物  的名稱為2,4-二乙基-6-丙基辛烷 的名稱為2,4-二乙基-6-丙基辛烷 | |
| B. | 月桂烯 (  )所有碳原子一定在同一平面上 )所有碳原子一定在同一平面上 | |
| C. | 取鹵代烴,加入氫氧化鈉的乙醇溶液加熱一段時間后冷卻,再加入稀硝酸酸化的硝酸銀溶液,一定會產生沉淀,并根據沉淀顏色判斷鹵代烴中鹵原子的種類 | |
| D. | 通常條件下,1mol的  分別與H2 和濃溴水完全反應時,消耗的H2和 分別與H2 和濃溴水完全反應時,消耗的H2和Br2的物質的量分別是 4mol、3mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
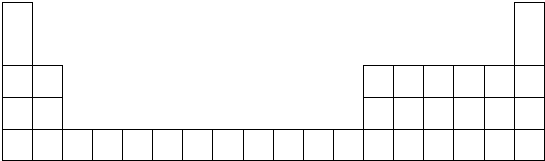
| 元素 | A | B | C | D | E | F | G | H |
| 原子半徑(nm) | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 | 0.152 | 0.037 | 0.099 |
| 主要化合價 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1,-1 | +7,-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 ;
;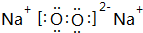 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ③④⑤ | B. | ①②③④⑤ | C. | ②③④ | D. | ②③④⑤⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該元素基態原子中共有13個電子 | B. | 該元素原子核外有3個電子層 | ||
| C. | 該元素原子最外層共有5個電子 | D. | 該元素原子L能層共有8個電子 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com