
分析 (1)鎂鋁合金與鹽酸發生反應的化學方程式為:Mg+2HCl=MgCl2+H2↑,2Al+6HCl=2AlCl3+3H2↑,n(H2)=$\frac{7.84L}{22.4L/mol}$=0.35mol,設出金屬的物質的量,根據質量、轉移電子守恒列方程式計算;
(2)根據HCl和氫氣之間的關系式計算鹽酸的物質的量,再根據c=$\frac{n}{V}$計算出該鹽酸的濃度.
解答 解:(1)鎂鋁合金與鹽酸發生反應的化學方程式為:Mg+2HCl=MgCl2+H2↑,2Al+6HCl=2AlCl3+3H2↑,n(H2)=$\frac{7.84L}{22.4L/mol}$=0.35mol,
設Mg的物質的量為x,Al的物質的量為y,根據金屬質量、轉移電子守恒列方程式:
$\left\{\begin{array}{l}{24x+27y=7.5}\\{2x+3y=0.35×2}\end{array}\right.$,
解得:$\left\{\begin{array}{l}{x=0.2mol}\\{y=0.1mol}\end{array}\right.$,
答:合金中鎂和鋁的物質的量分別是0.2mol、0.1mol;
(2)金屬與500mL鹽酸恰好反應,根據反應關系式2HCl~H2↑可知,500mL該鹽酸中含有氯化氫的物質的量為:0.35mol×2=0.7mol,
所以該鹽酸的物質的量濃度為:c(HCl)=$\frac{0.7mol}{0.5L}$=1.4mol/L,
答:所使用鹽酸的物質的量濃度為1.4mol/L.
點評 本題以鎂鋁合金為載體考查了混合物反應的計算,題目難度中等,根據各物質之間的關系式結合守恒思想分析解答,試題充分考查了學生的分析、理解能力及化學計算能力.


科目:高中化學 來源: 題型:解答題
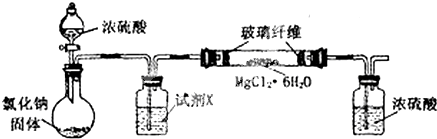
| 實驗序號 | 氯化鎂固體中氯元素含量/% | 溫度/℃ | 粉碎方式 | 催化效果/g•g-1 |
| 1 | 70.97 | 20 | 滾動球磨 | 3.9×104 |
| 2 | 74.45 | 20 | 滾動球磨 | 5.0×104 |
| 3 | 74.45 | 20 | 振動球磨 | 5.9×104 |
| 4 | ω | 100 | 振動球磨 | 6.5×104 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2的結構式: | |
| B. | 次氯酸的結構式為:H-Cl-O | |
| C. | 硫離子的核外電子排布式:1s22s22p63s23p6 | |
| D. | NH3的電子式: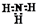 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下0.1mol•L-1的下列溶液中:①NH4Al(SO4)2;②NH4Cl;③CH3COONH4,c(NH4+)由大到小的順序為②>①>③ | |
| B. | 常溫下0.4mol•L-1CH3COOH溶液和0.2mol•L-1NaOH溶液等體積混合后溶液顯酸性,溶液中粒子濃度由大到小的順序為c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | 0.1mol•L-1 Na2CO3溶液與0.2mol•L-1NaHCO3溶液等體積混合所得溶液中:c(CO32-)+2c(OH-)═c(HCO3-)+3c(H2CO3)+2c(H+) | |
| D. | 0.1mol•L-1的氨水與0.05mol•L-1H2C2O4溶液等體積混合所得溶液中:c(NH4+)+c(NH3•H2O)═2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com