
| A. | 在氧化還原反應中,還原劑一定是失去電子的反應物 | |
| B. | 在氧化還原反應中,非金屬單質一定是氧化劑 | |
| C. | 某元素從化合態轉變為游離態時,該元素一定被還原 | |
| D. | 金屬陽離子被還原不一定得到金屬單質 |
分析 A.氧化劑、還原劑可能為同種物質;
B.非金屬單質可能為還原劑;
C.某元素從化合態轉變為游離態時,可能被氧化或被還原;
D.金屬陽離子被還原,可能為金屬陽離子.
解答 解:A.氧化劑、還原劑可能為同種物質,如氯氣與NaOH的反應中,氯氣失去電子也得到電子,故A錯誤;
B.非金屬單質可能為還原劑,如C與水蒸氣的反應中,C為還原劑,故B錯誤;
C.某元素從化合態轉變為游離態時,可能被氧化或被還原,如硫化氫與二氧化硫反應生成S,故C錯誤;
D.金屬陽離子被還原,可能為金屬陽離子,如鐵離子得到電子轉化為亞鐵離子,故D正確;
故選D.
點評 本題考查氧化還原反應,為高頻考點,把握反應中元素的化合價變化、基本概念等為解答的關鍵,側重分析與應用能力的考查,注意結合實例分析,題目難度不大.


科目:高中化學 來源: 題型:選擇題

| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,Cl2與NaOH溶液反應:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 澄清石灰水與少量小蘇打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 稀H2SO4與Ba(OH)2溶液反應:Ba2++OH-+H+十SO42-═BaSO4↓+H2O | |
| D. | 氯化亞鐵溶液中通入氯氣:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 陽離子 | Na+ Mg2+ Fe3+ Al3+ Fe2+ |
| 陰離子 | OH- CO32- Cl- NO3- SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
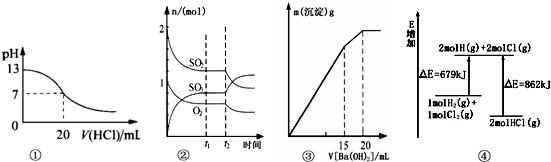
| A. | 圖①表示25℃時,用0.1 mol/L鹽酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH隨加入酸體積的變化得到的滴定曲線 | |
| B. | 圖②表示一定條件下進行的反應2SO2(g)+O2(g)?2SO3(g)△H<0各成分的物質的量變化,t2時刻改變的條件可能是降低溫度或縮小容器體積 | |
| C. | 圖③表示某明礬溶液中加入Ba(OH)2溶液,沉淀的質量與加入Ba(OH)2溶液體積的關系,在加入20 mL Ba(OH)2溶液時鋁離子恰好沉淀完全 | |
| D. | 圖④表示化學反應H2(g)+C12(g)═2HCl(g)的能量變化,則該反應的反應熱△H=﹢183 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 14 g乙烯和丙烯混合氣體中的氫原子數為NA | |
| B. | 1 mol N2與4 mol H2反應生成的NH3分子數小于2NA | |
| C. | 1 mol Fe溶于過量硝酸,電子轉移數為3NA | |
| D. | 標準狀況下,2.24 L CH4含有的共價鍵數為0.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 反應物 | 產物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | KClO3、濃鹽酸 | Cl2、… |
| A. | 第①組反應的其余產物為H2O和O2 | |
| B. | 第②組反應中Cl2與FeBr2的物質的量之比為1:2 | |
| C. | 第③組反應中還原產物是KCl,生成3 mol Cl2轉移電子6mol | |
| D. | 氧化性由強到弱順序為ClO3->Cl2>Br2>Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com