
| HX | HY | HZ | |
| ��� mol•L-1 | 0.1 0.5 | 1.0 1.5 | 2.0 2.5 |
| ��x�� | 0.3% 0.13% | 0.3% 0.24% | 0.5% 0.45% |
���� ��1��������x��늽��|����늽��|����ˮ��Һ�к����ڠ�B(t��i)�¶�����늵Ļ������Ƿ�늽��|��
��2���������Ƕ�Ԫ���ᣬ��ˮ��Һ�зֲ���x����һ����x����H+��HSO3-���������c�Ǐ�늽��|����ˮ��Һ����ȫ��x����ClO-��Na+��
��3����ͬ���|����늽��|��Һ�У���Һ���ԽС늽��|����x�̶�Խ��
��4������ͬ��B(t��i)�£���ͬ������x��Խ��������Խ����
��5�������淴��������ȕr���淴���_��ƽ���B(t��i)��ƽ���wϵ�и����|�����|���������|������ȡ��ٷֺ����Լ��ɴ������һϵ����������׃��
��� �⣺��1���ف�������Һ�ǻ����Ȳ���늽��|Ҳ���Ƿ�늽��|��
�ڴ������c�����}�����㏊늽��|��
���Ȼ�����w����ˮ��ȫ��x�����ڏ�늽��|��
�����������ڠ�B(t��i)�º�ˮ��Һ������܌�늣����ڻ�����Ƿ�늽��|��
�������^�����}�����ڠ�B(t��i)����ȫ��x�����ڏ�늽��|��
�ް��Ȿ��������x�������Ƅӵ��x�ӣ����ڻ�����Ƿ�늽��|��
�߱���������ˮ���ܲ�����x��������x�Ӻ͚��x�ӣ�������늽��|��
��������c���w�����}�����ڠ�B(t��i)����ˮ��Һ�������ȫ��x�����ڏ�늽��|��
��������F�������A��������x��������늽��|��
��NO2����������x�������Ƅӵ��x�ӣ����ڷ�늽��|���ʴ𰸞飺�ߢᣬ�ܢޢ⣻
��2���������Ƕ�Ԫ���ᣬ��ˮ��Һ�зֲ���x����һ����x����H+��HSO3-������x����ʽ��H2SO3?H++HSO3-��
�������c�Ǐ�늽��|����ˮ��Һ����ȫ��x����ClO-��Na+������x����ʽ��NaClO�TClO-+Na+��
�ʴ𰸞飺H2SO3?H++HSO3-��NaClO�TClO-+Na+��
��3��һˮ�ϰ�����늽��|������Һ�������xƽ�⣬��ˮ�ĝ��Խ��һˮ�ϰ�����x�̶�ԽС�����ԽС��һˮ�ϰ�����x�̶�Խ��
��ƿ��ˮ�ĝ������ƿ��ˮ�ĝ�ȵ�10��������늽��|�ĝ��ԽС����x�̶�Խ�ʼ�ƿ��ˮ����x�ȱ���ƿ��ˮ����x��С��
���Լס��҃�ƿ��ˮ��[OH-]֮��С��10���ʴ𰸞飺С�ڣ�
��4������x�ȴ�С��֪����HZ��HY��HX���ʴ𰸞飺HZ��HY��HX��
��5����ֻ�ж���������ɫ������Ϛ��w���ɫ���ٸ�׃�r���������������|������׃���f��ԓ�����_��ƽ���B(t��i)�������_��
�������w�e��׃����Ϛ��w�|����׃�����ԟoՓ�Ƿ��_��ƽ���B(t��i)����Ϛ��w�ܶ�ʼ�K��׃����Ϛ��w���ܶȲ��ٸ�׃�Ġ�B(t��i)��һ���_��ƽ�⣬���e�`��
�۷���ǰ����w����������Ϛ��w�ĉ������ٸ�׃�r��ԓ�����_��ƽ���B(t��i)�������_��
�ܷ���ǰ����w�����|�����������������������|���pС������Ϛ��w��ƽ�����������|�����ٸ�׃�r�������|�����|������׃�������_��ƽ���B(t��i)�������_��
�ݷ���ǰ��$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��c��{O}_{2}��}$�ı�ֵ�pС����$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��c��{O}_{2}��}$�ı�ֵ���ٸ�׃�r�����|�ĝ�Ȳ�׃�������_��ƽ���B(t��i)�������_��
���x���٢ۢܢݣ�
�c�u ���}�����^�C�ϣ��漰����늽��|�Дࡢ��늽��|��xƽ�⡢���Wƽ���B(t��i)�Д��֪�R�c������l���c�����ؿ���W�������Д༰������������������������_��ֻ�з���ǰ���׃����������׃�r���淴���_��ƽ���B(t��i)���ǽ��5���}���P�I���}Ŀ�y�Ȳ���



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ��2016-2017�W���������_�ЌW�߶��ϵ�һ���¿����Wԇ���������棩 �}�ͣ��x���}
�ڻ��W����A(g)��3B(g)  2C(g)��D(g)�У������|��ƽ�����������g���Pϵʽ���_����
2C(g)��D(g)�У������|��ƽ�����������g���Pϵʽ���_����
A��v(A)��v(B) B��v(A)��2v(C) C��3v(B)��v(C) D��v(B)��3v(D)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
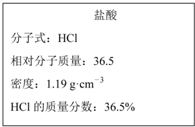 ��D�錍���ij���}��ԇ��ƿ�ϵĘ˺������P���ݣ�ԇ�����˺��ϵ����P�����ش����І��}��
��D�錍���ij���}��ԇ��ƿ�ϵĘ˺������P���ݣ�ԇ�����˺��ϵ����P�����ش����І��}���鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
 �Ҝ�����10mL 0.1mol•L-1 NaOH��Һ����μ���0.1mol•L-1��һԪ��HA����ҺpH��׃��������D��ʾ��
�Ҝ�����10mL 0.1mol•L-1 NaOH��Һ����μ���0.1mol•L-1��һԪ��HA����ҺpH��׃��������D��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
| ��̖ | �����}����w�e/mL | ���yKOH��Һ���w�e/mL |
| 1 | 27.23 | 25.00 |
| 2 | 28.24 | 25.00 |
| 3 | 27.25 | 25.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | �к�10mL 1 mol•L-1 CH3COOH��Һ��Ҫ10 mL 1 mol•L-1 NaOH��Һ | |
| B�� | ���|���������ͬ�r���\�����}�ᷴ�������ʱȸ����ᷴ�������ʿ� | |
| C�� | 0.01mol•L-1������Һ��pH����2 | |
| D�� | 0.1mol•L-1 CH3COONa��Һ�@�A�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | ���|������Ⱥ��w�e����ͬ���}��ʹ�����Һ�����c�����\�����r����ʼ�r���߮a��H2���ʻ������ | |
| B�� | 100mL1mol•L-1���}���50mL2mol•L-1���}�ᣬ�քe�c�������\�����r�����߷ų�H2���ʺ��|������� | |
| C�� | 100mLpH=3��H2SO4��HCl��Һ���c�����\�����ų�H2���|����� | |
| D�� | 100mLpH=3���}���c������Һ���c�����\����������H2���|����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | 2��3-�������� | B�� | 2-��-4-�һ�-1-��ϩ | ||
| C�� | 3-��-1-��ϩ | D�� | 3��3-����-2-��ϩ |
�鿴�𰸺ͽ���>>
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com