
廢舊無汞堿性鋅錳電池可用于制造隱形戰機的機身涂料MnxZn(1-x)Fe2O4,該電池工作反應原理為Zn+2MnO2+2H2O 2MnO(OH)+Zn(OH)2。某化學小組利用廢電池制涂料的工藝如下:
2MnO(OH)+Zn(OH)2。某化學小組利用廢電池制涂料的工藝如下:
A.浸取:將去除表面塑料的舊電池加入水中浸取并過濾,濾液經操作a得KOH固體;
B.溶液:濾渣中加入過量稀硫酸和足量雙氧水,至不再出現氣泡時,過濾;
C.測成分:測步驟B中濾液成分,然后加入鐵粉;
D.氧化:加入雙氧水氧化;
E.調pH:滴加氨水調pH,經結晶處理得MnxZn(1-x)Fe2O4。
(1)浸取時的操作有 ______。
A.拆解、粉碎舊電池 B.降低溫度 C.攪拌 D.加壓
(2)操作a為________。
(3)溶渣時生成Mn2+的主要離子方程式為______________________________。
(4)若步驟C測得濾液中金屬離子組成為:c(Mn2+) +c(Zn2+) =0.8mol/L, c(Fe2+ ) = 0. 1 mol/L。若濾液體積為lm3,要合成MnxZn(1-x)Fe2O4,需加入Fe粉質量為___________kg(忽略體積變化)。
(5)氧化時,因為分解所需雙氧水的量比理論值大得多。其原因可能是①溫度過高;②______。
(6)最后一步結晶時,處理不當易生成MnFe2O4和ZnFe2O4。要制得MnxZn(1-x)Fe2O4,最后一步結晶時需注意______________________。
(7)某小組構想用ZnSO4、MnSO4溶液為原料,以Fe作電極用電解法經過一系列步驟制得MnxZn(1-x)Fe2O4,則開始電解時陽極反應式為___________________________________。
科目:高中化學 來源:2017屆安徽省安慶市高三第二次模擬考試理科綜合化學試卷(解析版) 題型:選擇題
化學與生產、生活、社會密切相關,下列有關說法中正確的是
A. 煤炭經氣化、液化和干餾等處理后,可轉化為清潔能源
B. “綠蟻新醅酒,紅泥小火爐”,“新醅酒”即新釀的酒,在釀酒的過程中,葡萄發生了水解反應
C. 地溝油和礦物油的主要化學成分相同
D. 聚氯乙烯可以用作食品包裝袋
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省高二2月聯考化學試卷(解析版) 題型:選擇題
下列各離子組在指定的溶液中一定能大量共存的是
①常溫在c(H+)/c(OH-)=10-10溶液中:K+、Na+、CH3COO-、SO42﹣
②常溫pH=11的溶液中:CO32﹣、Na+、AlO2﹣、NO3﹣
③水電離出的H+濃度c(H+)=10﹣12mol•L?1的溶液中:Cl﹣、NO3﹣、Na+、S2O32﹣
④使甲基橙變紅色的溶液中:Fe3+、NO3﹣、Na+、SO42﹣
A.①②③ B.①②④ C.②③④ D.①③④
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省棗莊市南校區高一3月月考化學試卷(解析版) 題型:選擇題
兩種微粒的質子數和電子數均分別相等,它們不可能是
A. 一種陽離子和一種陰離子
B. 一種單質和一種化合物分子
C. 兩種不同的分子
D. 一種原子和一種分子
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省棗莊市南校區高一3月月考化學試卷(解析版) 題型:選擇題
下列化合物中陽離子半徑與陰離子半徑之比最大的是
A. LiI B. NaBr C. KCl D. CsF
查看答案和解析>>
科目:高中化學 來源:2017屆四川省成都市高三第二次模擬考試理綜化學試卷(解析版) 題型:選擇題
下列選項中,利用相關實驗器材(規格和數量不限)能夠完成相應實驗的是
選項 | 實驗器材 | 相應實驗 |
A | 試管、鐵架臺、導管 | 乙酸乙酯的制備 |
B | 錐形瓶、漏斗、雙孔塞、導管、帶余燼的木條、藥匙 | 檢驗MnO2對H2O2分解速率的影響 |
C | 500mL容量瓶、燒杯、玻璃棒、天平 | 配制 500mL1.00mol/LNaCl溶液 |
D | 三腳架、坩堝、酒精燈、坩堝鉗 | 鈉在空氣中燃燒 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高一下學期第一次月考化學試卷(解析版) 題型:填空題
用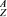 X表示原子:
X表示原子:
(1)中性原子的中子數:N=________。
(2)陽離子的中子數:AXn+共有x個電子,則N=________。
(3)陰離子的中子數:AXn-共有x個電子,則N=________。
(4)中性分子中子數:12C18O2分子中,N=________。
(5)A2-原子核內有x個中子,其質量數為m,則n gA2-所含電子的物質的量為________mol。
(6)某元素的同位素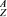 X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反應。若這種同位素原子核內有20個中子,則:
X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反應。若這種同位素原子核內有20個中子,則:
①Z值和A值:Z=________,A=________;
②X元素在周期表中的位置_____________________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高一下學期第一次月考化學試卷(解析版) 題型:選擇題
下列過程中,共價鍵被破壞的是
A.碘升華 B.溴蒸氣被木炭吸附
C.酒精溶于水 D.HCl氣體溶于水
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省成都簡陽市高一上學期期末檢測化學試卷(解析版) 題型:實驗題
為了探究木炭與濃H2SO4反應的產物中是否存在CO2,某同學選用如圖所示裝置進行實驗:
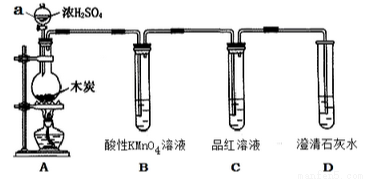
(1)儀器a的名稱為:__________;在組裝好上述實驗裝置后,在裝入藥品之前必需的實驗操作是________________。
(2)寫出A中發生反應的化學方程式____________________。該裝置還可以用于實驗室制取Cl2,請寫出實驗室制取Cl2的離子方程式并用單線橋標明電子轉移________________。
(3)裝置B的作用是____________________。
(4)能說明產物中一定存在CO2氣體的實驗現象為________________。
(5)質量分數為98%的濃硫酸,其密度為1.84g/ml,該濃硫酸的物質的量濃度為__________,用該硫酸配制500ml 0.5mol/L的稀硫酸,主要儀器除量筒、燒杯、玻璃棒、膠頭滴管外,還需要____________,定容時由于俯視刻度線,則對濃度產生的影響為___________ (填“偏大”“偏小”或“無影響”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com