
| 金屬 | Na | Cu | Al | Fe |
| 熔點/℃ | 97.5 | 1 083 | 660 | 1 535 |
| 沸點/℃ | 883 | 2 595 | 2 200 | 3 000 |
| A. | Cu與Na | B. | Fe與Cu | C. | Fe與Al | D. | Al與Na |
分析 由合金的形成可知,兩種金屬若能夠形成合金,則熔點較高的金屬的熔點不能大于熔點較低的金屬的沸點.
解答 解:合金是不同種金屬在熔化狀態下形成的一種熔合物,即兩種金屬都成為液態時進行混合;
A.由于金屬Na的沸點較低,Cu的熔點高于Na的沸點,在鐵熔化時溫度達1535℃,而此時金屬Na已變成氣態,無法完成液態時混合,故Cu和Na不能形成合金,故A正確;
B.鐵的熔點低于鋁的沸點,兩種金屬能夠形成合金,故B錯誤;
C.鐵的熔點低于銅的沸點,兩種金屬能夠形成合金,故C錯誤;
D.鋁的熔點低于鈉的沸點,兩種金屬能夠形成合金,故D錯誤;
故選A.
點評 本題考查了合金的形成條件,題目難度不大,注意制造合金時,兩種金屬必須都是液態才能制成合金,一種液態、一種氣態不會轉化成合金.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
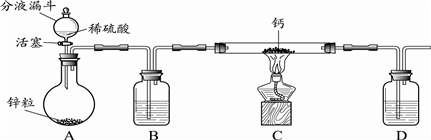
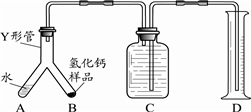
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
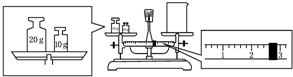 實驗室欲用NaOH固體配制1.0mol•L-1的NaOH溶液245mL:
實驗室欲用NaOH固體配制1.0mol•L-1的NaOH溶液245mL:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 與H2化合能力:At2>I2 | B. | 砹在常溫下為白色固體 | ||
| C. | 砹原子的最外電子層上有7個電子 | D. | 砹能從NaCl溶液中置換出氯單質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
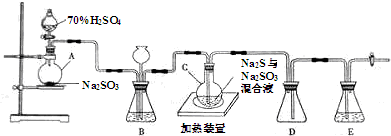
| 第一份 | 第二份 | 第三份 | |
| 樣品的質量/g | 12.60 | 18.90 | 28.00 |
| 二氧化硫的體積/L | 1.12 | 1.68 | 2.24 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 編號 | 實驗操作 | 目的 |
| A | 取4gNaOH固體溶于100mL水中 | 配制0.1mol•L-1NaOH溶液 |
| B | 向沸水中逐滴加入1-2mLFeCl3飽和溶液,攪拌并繼續煮沸到變成紅褐色 | 制備Fe(OH)3膠體 |
| C | 測定等物質的量濃度的鹽酸、硝酸的pH | 比較Cl、N的非金屬性 |
| D | 用MgCl2、AlCl3溶液做導電性試驗 | 證明兩者是離子化合物還是共價化合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向50 mL 1 mol•L-1明礬溶液中滴入少量0.1 mol•L-1Ba(OH)2溶液Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ | |
| B. | 已知還原性Fe2+>Br-,a mol FeBr2溶液中通入a mol Cl2:2Fe2++2Br-+2Cl2═Br2+2Fe3++4C1- | |
| C. | 向KI與稀硫酸的混合溶液中通入氧氣:4H++O2+6I-═3I2+2H2O | |
| D. | 在澄清石灰水中加入適量碳酸氫鎂溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 鐵及其化合物在生活、生產中有廣泛應用.請回答下列問題:
鐵及其化合物在生活、生產中有廣泛應用.請回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com