
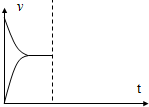
 在537℃、1.01×105Pa時,往容積可變的密閉容器中充入1mol X和3mol Y,此時容積為V L.保持恒溫恒壓,發生反應X(g)+3Y(g)?2Z(g),達到平衡時,平衡混合氣體中Z的體積分數為0.5.
在537℃、1.01×105Pa時,往容積可變的密閉容器中充入1mol X和3mol Y,此時容積為V L.保持恒溫恒壓,發生反應X(g)+3Y(g)?2Z(g),達到平衡時,平衡混合氣體中Z的體積分數為0.5.分析 恒壓下 X(g)+3Y(g)$\stackrel{\;}{?}$2Z(g),
開始 1 3 0
轉化 x 3x 2x
平衡1-x 3-3x 2x
到平衡時,平衡混合氣體中Z的體積分數為0.5,
則$\frac{2x}{4-2x}$=0.5,解得x=$\frac{2}{3}$mol,以此結合等效平衡來解答該題.
解答 解:恒壓下 X(g)+3Y(g)$\stackrel{\;}{?}$2Z(g),
開始 1 3 0
轉化 x 3x 2x
平衡 1-x 3-3x 2x
到平衡時,平衡混合氣體中Z的體積分數為0.5,
則$\frac{2x}{4-2x}$=0.5,解得x=$\frac{2}{3}$mol,
(1)X的轉化率約為$\frac{\frac{2}{3}mol}{1mol}$×100%=66.7%,在其他條件不變時,再通入1mol X和3mol Y的混合氣體,由于壓強不變,則速率不變,圖象為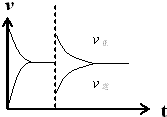 ,
,
故答案為:66.7%; ,;
,;
(2)保持上述溫度和壓強恒定不變,若向容器中只充入4molZ,與上述平衡等效,則Y的體積分數為$\frac{3-3×\frac{2}{3}}{4-2×\frac{2}{3}}$×100%=37.5%,
由物質的量與體積成正比可知,設平衡的體積為x,則$\frac{4}{V}=\frac{\frac{8}{3}×2}{x}$,解得x=$\frac{4V}{3}$L,故答案為:37.5%;$\frac{4V}{3}$;
(3)容積固定不變的密閉容器,仍控制溫度不變,使2mol X和6mol Y反應,達到平衡時平衡氣體中Z的體積分數仍為0.5,
與加入4molZ建立的平衡等效,體積為$\frac{4V}{3}$L,故答案為:$\frac{4V}{3}$;
(4)容器體積保持VL不變(恒容),往其中充入a mol X的b mol Y,使反應達到平衡,這時平衡氣體中Z的體積分數仍為0.5,體系壓強為1.01×105Pa,若a:b=1:3,則 X(g)+3Y(g)$\stackrel{\;}{?}$2Z(g),
開始 a 3a 0
轉化 x 3x 2x
平衡a-x 3a-3x 2x
到平衡時,平衡混合氣體中Z的體積分數為0.5,
$\frac{2x}{4a-2x}$=0.5,4a-2x=4mol,
解得a=1.5mol,故答案為:1.5mol.
點評 本題考查化學平衡的計算及等效平衡,為高頻考點,側重于學生的分析、計算能力的考查,注意化學平衡三段法的計算及等效平衡的條件、體積與物質的量的關系即可解答,題目難度較大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
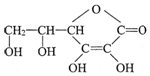 ,分子式為C6H8O6;其中的-OH叫羥基(填官能團名稱).在維生素C溶液中滴入少量藍色的含有淀粉的碘水,可觀察到的現象是藍色褪去,說明維生素C有還原性(填氧化性或還原性).
,分子式為C6H8O6;其中的-OH叫羥基(填官能團名稱).在維生素C溶液中滴入少量藍色的含有淀粉的碘水,可觀察到的現象是藍色褪去,說明維生素C有還原性(填氧化性或還原性).查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

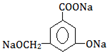 .
.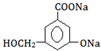 .
.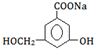 .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
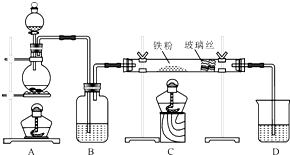 工業上,向500℃~600℃的鐵屑中通入氯氣生產無水氯化鐵(已知熾熱鐵屑與氯化氫生成氯化亞鐵).現用如圖所示的裝置模擬上述過程進行試驗.
工業上,向500℃~600℃的鐵屑中通入氯氣生產無水氯化鐵(已知熾熱鐵屑與氯化氫生成氯化亞鐵).現用如圖所示的裝置模擬上述過程進行試驗.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
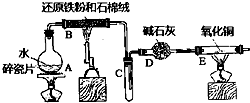 某校化學小組學生利用如圖所列裝置進行“鐵與水反應”的實驗,并進行了其他有關實驗.(圖中夾持及尾氣處理裝置均已略去)
某校化學小組學生利用如圖所列裝置進行“鐵與水反應”的實驗,并進行了其他有關實驗.(圖中夾持及尾氣處理裝置均已略去)查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用催化劑能加快反應速率 | |
| B. | 壓強增大不影響化學反應速率 | |
| C. | 冬天氣溫低,反應速率降低,對人類危害減小 | |
| D. | 無論外界條件怎樣改變,均對此化學反應的速率無影響 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com