
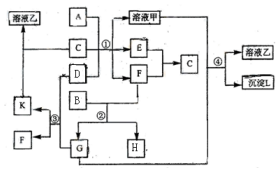
 如圖表示常見的單質及其化合物之間的轉化關系,其中A為常見的金屬單質,B為非金屬單質(一般是黑色粉末),C是常見的無色無味液體,D是淡黃色的固體化合物.(反應條件圖中已省略).
如圖表示常見的單質及其化合物之間的轉化關系,其中A為常見的金屬單質,B為非金屬單質(一般是黑色粉末),C是常見的無色無味液體,D是淡黃色的固體化合物.(反應條件圖中已省略).分析 C是常見的無色無味液體,C為H2O,D是淡黃色的固體化合物,則D為Na2O2,二者反應生成氫氧化鈉,A為常見的金屬單質,由轉化關系可知A為Al,B為非金屬單質,一般是黑色粉末,則B為碳,由反應①可知甲為NaAlO2,E、F分別為O2和H2中的一種,B能與F反應生成G與H,且G能與過氧化鈉反應生成F與K,可推知F為O2,E為H2,G為CO2,H為CO,K為Na2CO3,由反應④可知L為Al(OH)3,溶液乙為Na2CO3溶液,以此解答該題.
解答 解:(1)C、D反應后的溶液為氫氧化鈉溶液,加入鋁,反應生成偏鋁酸鈉和氫氣,方程式為2Al+2 NaOH+2H2O=2NaAlO2+3H2↑,
故答案為:2Al+2 NaOH+2H2O=2NaAlO2+3H2↑;
(2)B為碳,F為O2,如二者按1:1反應,則生成CO2,按2:1反應,則生成CO,如物質的量之比為4:3,則同時生成CO和CO2,則G為CO2,可與碳酸鈉溶液反應,而H為CO,故答案為:CO2; CO;
(3)反應④的離子方程式為:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,故答案為:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-.
點評 本題考查無機物的推斷,為高考常見題型,難度中等,注意充分利用轉化關系中物質均為短周期元素組成,結合題目信息中A為常見金屬及物質的顏色、轉化關系中特殊反應進行推斷,需要學生熟練掌握元素化合物知識.


 寒假學與練系列答案
寒假學與練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,11.2LHF所含的分子數為0.5NA | |
| B. | 常溫下,100mL2mol/L的明礬溶液凈水時,生成具有凈水作用的微粒數為0.2NA | |
| C. | 常溫下,1L0.1mol/LNH4NO3溶液中氧原子數為0.3NA | |
| D. | 標準狀況下,4.2gCH2=CH2和CH3CH=CH2的混合氣體中所含有的氫原子數為0.6NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硅晶體廣泛應用于電子工業的各個領域 | |
| B. | 氧化鎂是優質的耐高溫材料 | |
| C. | 明礬凈水劑正逐步被含鐵凈水劑所取代 | |
| D. | 用鋁制餐具長時間存放堿性食物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③⑥ | B. | ②③⑥⑧ | C. | ①④⑤⑦ | D. | ①②③⑦ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | △H2>△H3 | B. | △H1<△H3 | C. | △H1+△H3=△H2 | D. | △H1+△H2>△H3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁能夠穩定存在于空氣中,而鐵很容易生銹,說明鐵比鋁活潑 | |
| B. | 等物質的量的Al、Fe分別與足量鹽酸反應放出等質量的H2 | |
| C. | 二者的氫氧化物都不可以通過氧化物化合反應直接制備 | |
| D. | 二者的單質都能與強堿溶液反應生成H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硅是良好的半導體材料 | |
| B. | 二氧化硅能與石灰石反應:SiO2+CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaSiO3+CO2↑ | |
| C. | 可以用焦炭還原二氧化硅生產硅:SiO2+2C$\frac{\underline{\;高溫\;}}{\;}$Si+2CO↑ | |
| D. | 水泥的主要成分是 Na2SiO3、CaSiO3 和 SiO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
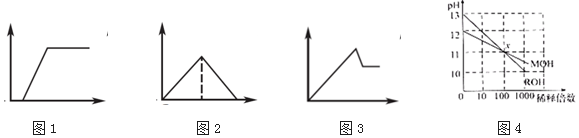
| A. | 圖1:往Na2CO3和NaOH混合液中逐滴加入鹽酸,產生氣體體積與鹽酸的物質的量的關系 | |
| B. | 圖2:往澄清石灰水中通入過量CO2氣體,產生沉淀質量與CO2的物質的量的關系 | |
| C. | 圖3:往AlCl3和MgCl2混合液中逐滴加入NaOH溶液,產生沉淀質量與NaOH溶液的物質的量的關系 | |
| D. | 圖4:若MOH和ROH表示兩種一元堿,則ROH的堿性強于MOH |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com