
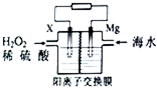
 交通運輸部在南海華陽礁舉行華陽燈塔和赤燈塔竣工發光儀式,宣布兩座大型多功能燈塔正式發光并投入使用.燈塔可用鎂海水電池提供能源,其裝置如圖所示.下列有關海水電池的說法正確的是( )
交通運輸部在南海華陽礁舉行華陽燈塔和赤燈塔竣工發光儀式,宣布兩座大型多功能燈塔正式發光并投入使用.燈塔可用鎂海水電池提供能源,其裝置如圖所示.下列有關海水電池的說法正確的是( )| A. | X可為鐵、銅、石墨等電極,發生氧化反應 | |
| B. | 每轉移2 mol電子,2molH+由交換膜左側向右側遷移 | |
| C. | 該電池能將化學能全部轉化成電能 | |
| D. | 正極的電極反應式為比O2+2e-+2H+═2H2O |
分析 該海水電池的負極材料是金屬鎂,發生失電子的氧化反應,正極材料的金屬活潑性比金屬鎂的差,該電極上發生得電子的還原反應,原電池是將化學能轉化為電能的裝置,根據電子守恒以及電子轉移知識來回答判斷.
解答 解:A、該海水電池的負極材料是金屬鎂,正極X的材料的金屬活潑性比金屬鎂的差,但是不能是可以和雙氧水之間反應的金屬鐵等物質,故A錯誤;
B、陽離子會移向正極,即每轉移2 mol電子,2molH+由交換膜右側向左側遷移,故B錯誤;
C、該電池能將化學能部分轉化成電能,部分轉化為熱能,故C錯誤;
D、原電池的正極上發生得電子的還原反應:H2O2+2e-+2H+═2H2O,故D正確;
故選D.
點評 總結題技巧總結:電極類型的判斷首先在明確屬于電解池還是原電池基礎上來分析的,原電池對應的是正、負兩極,電解池對應的陰、陽兩極,根據元素價態變化找出氧化劑與還原產物即可解答.


科目:高中化學 來源: 題型:選擇題
| A. | 水電解生成氫氣和氧氣,說明水中含有氫分子和氧分子 | |
| B. | 用肥皂水不可以區分硬水和軟水 | |
| C. | 將黃河水經沉降、過濾、吸附,滅菌等凈化操作后,可供人們生活用水 | |
| D. | 水體有一定的自凈功能,部分工業污水可直接排放 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{a+b}{4}$ | B. | 4(3a+b) | C. | 4(a+b) | D. | $\frac{3a+b}{4}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 地球上99%溴蘊藏在大海中,故溴被稱為“海洋元素” | |
| B. | 高壓鈉燈發出的黃光射程特別遠,故常用于道路與廣場的照明 | |
| C. | 碳酸氫鈉可與鹽酸反應,故可作治療胃酸過多的藥劑 | |
| D. | 利用光線在硅晶體內的全反射現象,可以制備光導纖維 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe在一定條件下與水反應生成H2和Fe(OH)3 | |
| B. | Fe3O4溶于鹽酸后加入幾滴KSCN溶液,溶液不顯血紅色 | |
| C. | FeCl2溶液蒸干后得到的是Fe(OH)3固體 | |
| D. | 將FeCl3飽和溶液滴入NaOH溶液中可制備Fe(OH)3膠體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖,密閉容器內分別充入空氣和H2、O2的混合氣體在可移動的活塞兩邊,在標準狀況下,若將H2、O2的混合氣體點燃引爆,活塞先左彈,恢復原溫度后,活塞右滑停留于容器的中央,則關于原來H2、O2的體積比下列正確的是( )
如圖,密閉容器內分別充入空氣和H2、O2的混合氣體在可移動的活塞兩邊,在標準狀況下,若將H2、O2的混合氣體點燃引爆,活塞先左彈,恢復原溫度后,活塞右滑停留于容器的中央,則關于原來H2、O2的體積比下列正確的是( )| A. | 4:17 | B. | 3:7 | C. | 8:13 | D. | 7:4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4LNO與11.2LO2混合,混合氣體所含分子數為NA | |
| B. | 1molAl3+含有的核外電子數為10NA | |
| C. | 常溫常壓下,1mol氮氣含有的原子總數為2NA | |
| D. | 1L1mol/LFeCl3溶液全部制成膠體,其中含膠粒的數目小于NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 滴加鹽酸時,HCl是還原劑,Cl2是還原產物 | |
| B. | 已知Bi為第ⅤA族元素,上述實驗說明Bi具有較強的非金屬性 | |
| C. | 若有0.1 mol NaBiO3參加了反應,則整個過程轉移電子0.4NA | |
| D. | 此實驗條件下,物質的氧化性:KMnO4>NaBiO3>Cl2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com