

| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 開始沉淀時 | 3.4 | 6.3 | 2.7 |
| 完全沉淀時 | 5.2 | 9.7 | 3.2 |
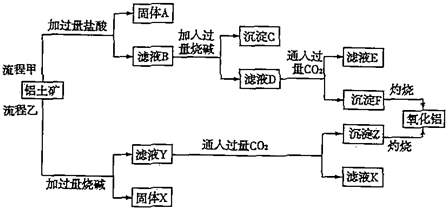
分析 鋁灰(含Al2O3及少量SiO2和FeO•xFe2O3),加入過量稀硫酸酸溶過濾,濾液為硫酸鋁、硫酸亞鐵、硫酸鐵,濾渣為二氧化硅和不溶性雜質,濾液中加入稍過量的高錳酸鉀溶液氧化亞鐵離子為鐵離子,調節溶液PH使鐵離子全部沉淀,鋁離子不沉淀,加入適量硫酸錳除去過量的高錳酸鉀過濾得到二氧化錳固體和氫氧化鐵沉淀,濾液主要是硫酸鋁溶液,蒸發濃縮,冷卻結晶過濾洗滌得到硫酸鋁晶體,
(1)氧化鋁是兩性氧化物溶于強酸強堿,與硫酸反應生成硫酸鋁和水;
(2)亞鐵離子、鐵離子同時存在,可用酸性高錳酸鉀溶液檢驗亞鐵離子;
(3)一定條件下,MnO4-可與Mn2+反應生成MnO2;
①依據金屬陽離子沉淀開始和完全沉淀需要的溶液pH分析,亞鐵離子被氧化為鐵離子,調節溶液pH使鐵離子全部沉淀;
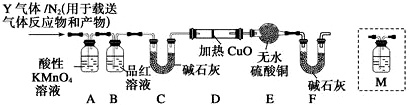
②濃鹽酸和二氧化錳再加熱條件下生成黃綠色氣體氯氣;
③加入MnSO4至紫紅色消失,目的是除去過量高錳酸根離子;
(4)由元素守恒可知,母液中存在較多的K+、SO42-.
解答 解:向鋁灰中加入過量稀H2SO4,A12O3和少量FeO•xFe2O3和硫酸反應生成硫酸鋁、硫酸鐵、硫酸亞鐵,SiO2不反應,過濾除去二氧化硅;向濾液中加入過量KMnO4溶液,高錳酸鉀把亞鐵離子氧化成鐵離子,調節溶液的pH約為3.7生成氫氧化鐵沉淀,除去鐵離子,過濾,濾液中含鋁離子和過量的高錳酸根離子,加入硫酸錳把過量高錳酸根離子除去,再過濾,對濾液蒸發濃縮、結晶分離出硫酸鋁晶體,
(1)硫酸溶解氧化鋁生成硫酸鋁和水,反應的離子方程式為:Al2O3+6H+=2Al3++3H2O,
故答案為:Al2O3+6H+=2Al3++3H2O;
(2)由于鐵離子和亞鐵離子同時存在,所以檢驗亞鐵離子應該用酸性高錳酸鉀溶液,方法為:取少量濾液,滴加KMnO4溶液,KMnO4溶液褪色,
故答案為:取少量濾液,滴加KMnO4溶液,KMnO4溶液褪色;
(3)①向濾液中加入過量KMnO4溶液,目的是氧化亞鐵離子為三價鐵離子;
依據圖表數據分析可知,鐵離子開始沉淀和沉淀完全的溶液PH為2.7~3.2,鋁離子和亞鐵離子開始沉淀的溶液pH大于3.2,所以調節溶液的pH約為3.2,可以使鐵離子全部沉淀,鋁離子不沉淀分離,
故答案為:將Fe2+氧化為Fe3+;調節pH值使鐵元素沉淀完全;
②向Ⅱ的沉淀中加入濃HCl并加熱,二氧化錳和濃鹽酸在加熱條件下反應MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,生成氯化錳、氯氣和水,生成的氯氣是黃綠色氣體,能說明沉淀中存在MnO2的現象是生成黃綠色氣體,
故答案為:有黃綠色氣體生成;MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
③MnO4-可與Mn2+反應生成MnO2,過濾除去,所以可以利用MnSO4的溶液和高錳酸鉀溶液反應生成二氧化錳,把過量高錳酸根離子除去,
故答案為:除去過量的MnO4-;
(4)反應后,溶液中存在較多的K+、SO42-便留在母液中,可回收的主要物質為K2SO4,
故答案為:K2SO4.
點評 本題考查了物質的制備流程分析,題目難度中等,涉及鋁、鐵及其化合物性質的應用,主要是混合物分離的方法和實驗設計,加入氧化劑氧化亞鐵離子,調節溶液PH是沉淀分離是解題的關鍵,試題充分考查了學生的分析、理解能力及化學實驗能力.


 習題精選系列答案
習題精選系列答案科目:高中化學 來源: 題型:選擇題
 如圖是M、N兩種不含結晶水的固體物質溶解度曲線.下列說法中正確的是( )
如圖是M、N兩種不含結晶水的固體物質溶解度曲線.下列說法中正確的是( )| A. | t1℃時,N比M的溶解度大 | |
| B. | 溫度從t1℃升高到t3℃時,N的飽和溶液張溶質的質量分數將增大 | |
| C. | M比N的溶解度大 | |
| D. | N中含有少量M時,可用降溫結晶法提純N |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在pH=3的溶液中:Na+、NO3-、Cl-、Al3+ | |
| B. | 使pH試紙呈紅色的溶液中:Fe2+、ClO-、SO42-、Na+ | |
| C. | 由水電離出的c(H+)=10-13 mol•L-1的溶液中:CO32-、SO42-、Cl-、Na+ | |
| D. | 加入鋁粉后產生大量氫氣的溶液中:NH4+、Na+、SO42-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 僅有②④⑥ | B. | 僅有①⑤⑦⑨⑩ | C. | 僅有②③④ | D. | 僅有①⑤⑥⑦⑨⑩ |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 化學鍵的斷裂和形成是物質在化學反應中發生能量變化的主要原因 | |
| B. | 水分解生成氫氣跟氧氣的同時吸收能量 | |
| C. | 1mol H2跟$\frac{1}{2}$mol O2反應生成1mol H2O釋放能量一定為245kJ | |
| D. | 為開發氫能,可研究設法將太陽能聚焦,產生高溫使水分解產生氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 非金屬性X>Y>Z | |
| B. | X、Y、Z形成的陰離子還原性逐漸增強 | |
| C. | 原子半徑X<Y<Z | |
| D. | X、Y、Z的氣態氫化物穩定性由弱到強 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com