
| A. | $\frac{ad}{22400}$mol/L | B. | $\frac{ad}{22400+36.5a}$mol/L | ||
| C. | $\frac{1000ad}{22400+36.5a}$mol/L | D. | $\frac{1000ad}{22.4+36.5a}$mol/L |
分析 根據n=$\frac{V}{{V}_{m}}$計算HCl的物質的量,根據m=nM計算HCl質量,根據m=dV計算水的質量,溶液質量=水的質量+HCl的質量,根據V=$\frac{m}p9vv5xb5$計算溶液體積,再根據c=$\frac{n}{V}$計算鹽酸的物質的量濃度.
解答 解:標況下,aL HCl的物質的量為$\frac{aL}{22.4L/mol}$=$\frac{a}{22.4}$mol,
HCl質量為$\frac{a}{22.4}$mol×36.5g/mol=$\frac{36.5a}{22.4}$g,
水的質量為1000mL×1g/mL=1000g,溶液質量=(1000+$\frac{36.5a}{22.4}$)g,
溶液體積=$\frac{(1000+\frac{36.5a}{22.4})g}{1000dg/L}$=$\frac{22400+36.5a}{22400d}$L,
該鹽酸的物質的量濃度為$\frac{\frac{a}{22.4}mol}{\frac{22400+36.5a}{22400d}L}$=mol/L=$\frac{1000ad}{22400+36.5a}$mol/L,
故選C.
點評 本題考查物質的量濃度計算,注意對定義式的理解掌握,關鍵是計算溶液體積,題目難度不大.


科目:高中化學 來源:2016-2017學年山東省德州市高二上10月月考化學試卷(解析版) 題型:選擇題
如圖為直流電源電解稀Na2SO4水溶液的裝置,通電后在石墨電極a和b附近分別滴加石蕊溶液,下列實驗現象正確的是( )
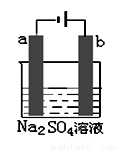
A.逸出氣體的體積:a電極的小于b電極的
B.a電極附近呈藍色,b電極附近呈紅色
C.a電極附近呈紅色,b電極附近呈藍色
D.電極逸出無味氣體,另一電極逸出刺激性氣味氣體
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HCl和NaOH反應的中和熱△H=-57.3 kJ•mol-1,則H2SO4和Ca(OH)2反應的中和熱△H=2×(-57.3)kJ•mol-1 | |
| B. | CO(g)的燃燒熱是283.0kJ/mol,則2CO2(g)═2CO(g)+O2(g)反應的△H=+586.0kJ•mol-1 | |
| C. | 需要加熱才能發生的反應一定是吸熱反應 | |
| D. | 1mol甲烷燃燒生成氣態水和二氧化碳所放出的熱量是甲烷燃燒熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 與金屬鈉反應:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | |
| B. | 與氧氣的燃燒反應:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | |
| C. | 與氧氣的催化氧化:CH3CH2OH+3O2$\stackrel{點燃}{→}$2CO2+3H2O | |
| D. | 與乙酸的酯化反應:CH3COOH+CH3CH2OH$\frac{\underline{\;濃硫酸\;}}{△}$CH3COOCH2CH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 反應過程中MnO2作催化劑 | B. | 鹽酸未完全反應 | ||
| C. | 參加反應的鹽酸有一半被氧化 | D. | 反應產生2.24L氯氣(標況) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上第一次月考化學試卷(解析版) 題型:選擇題
在25℃時,密閉容器中X、Y、Z三種氣體的初始濃度和平衡濃度如下表:
物質 | X | Y | Z |
初始濃度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡濃度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列說法錯誤的是( )
A.反應達到平衡時,X的轉化率為50%
B.反應可表示為X+3Y 2Z,其平衡常數為1600
2Z,其平衡常數為1600
C.改變溫度可以改變此反應的平衡常數
D.增大壓強使平衡向生成Z的方向移動,平衡常數增大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com