
某化學小組為測定一瓶失去標簽的鹽酸的溶質質量分數,分成甲、乙兩組,分別用不同的方法進行測定.
實驗設計:
甲組:取純凈碳酸鈣粉末5g于燒杯中,加入20g該鹽酸溶液,充分反應后,過濾、洗滌、干燥,稱量得剩余固體3g.
乙組:取純凈碳酸鈣粉末5g于錐形瓶中,將20g該鹽酸溶液加入分液漏斗,利用測定產生二氧化碳的體積(20℃、標準大氣壓)計算鹽酸濃度.裝置示意圖如圖:
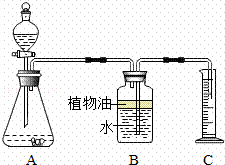
數據處理:
(1)請利用甲組數據計算該鹽酸的溶質質量分數.(寫出計算過程)
(2)乙組計算結果略小于甲組.經過多次實驗仍得到相同結果(忽略量筒引起的誤差),可能的原因是 .
答案 分析:
(1)根據剩余固體3g,可知碳酸鈣的質量為2g,將碳酸鈣的質量代入化學反應方程式來計算氯化氫的質量,再計算鹽酸的質量分數;
(2)利用測定產生二氧化碳的體積(20℃、標準大氣壓)計算鹽酸濃度,計算結果略小于甲組,可能是測量的水的體積小于生成氣體的體積; B、C之間的導管內實驗前無水,實驗后有水;內外氣壓相同時,二氧化碳無法將相應體積的水壓入量筒;二氧化碳可能溶解在A中反應后的溶液中等.
解答:
解:
(1)設參加反應的HCl質量為x,消耗碳酸鈣質量為5g﹣3g=2g
2HCl+CaCO3=CaCl2+H2O+CO2↑
73 100
x 2g
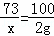
X=1.46g
鹽酸的溶質質量分數為: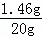 ×100%=7.3%
×100%=7.3%
(2)測量的水的體積小于生成氣體的體積; B、C之間的導管內實驗前無水,實驗后有水;內外氣壓相同時,二氧化碳無法將相應體積的水壓入量筒;二氧化碳可能溶解在A中反應后的溶液中.
答案:
(1)鹽酸的溶質質量分數為7.3%;
(2)內外氣壓相同時,二氧化碳無法將相應體積的水壓入量筒.


科目:初中化學 來源: 題型:
化學與生活息息相關,請你用所學化學知識回答以下生活中的問題。
(1)小明放學一進家門就聞到菜香,這證明了微粒具有 性質。
(2)加碘食鹽中的“碘”是指 (填“單質”或“元素”)。
(3)自來水廠凈水過程中常用活性炭,活性炭的主要作用是 。
(4)膨化食品包裝時常通入空氣主要成分之一的 氣體以防止該食品變質和壓碎,該氣體是______。
氣體以防止該食品變質和壓碎,該氣體是______。
(5)若廚房失火時,移走“煤氣罐”,這是利用了 原理滅火。
查看答案和解析>>
科目:初中化學 來源: 題型:
請你各舉一例,說明下列有關溶液的敘述是錯誤的。
(1)溶液一定是無色的。
實例: 溶液不是無色的。
(2)均一、穩定的液體都是溶液。
實例: 是液體,但不是溶液。
(3)溶液的溶質一定是固體。
實例: 可做溶質,但不是固體。
查看答案和解析>>
科目:初中化學 來源: 題型:
根據反應事實可以推出影響化學反應的因素,下列推理中不合理的是( )
| 選項 | 化學反應事實 | 影響因素 |
| A | 蠟燭在純氧中燃燒的火焰比在空氣中燃燒的火焰更明亮 | 反應物濃度 |
| B | 煤粉比煤塊燃燒的更加劇烈、更加充分 | 反應物種類 |
| C | 碳在常溫下不與氧氣反應,點燃時能與氧氣反應 | 反應溫度 |
| D | 雙氧水在通常情況下難分解,加入二氧化錳后迅速分解 | 催化劑 |
查看答案和解析>>
科目:初中化學 來源: 題型:
乙醇是一種清潔能源。乙醇的燃燒可發生以下兩個反應:
①C2H6O+3O2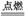 2CO2+3H2O
2CO2+3H2O
②aC2H6O+5O2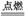 2CO2+2CO+6H2O
2CO2+2CO+6H2O
試填空:(1)反應②中的化學計量數a=________。
(2)反應____________(填序號)屬于完全燃燒,產物無毒性。
(3)9.2 g乙醇在空氣中若按化學方程式②發生反應,生成一氧化碳的質量為________g。
查看答案和解析>>
科目:初中化學 來源: 題型:
為了測定實驗室中氯酸鉀樣品的純度,某學習小組取2.5g該樣品與0.5g二氧化錳混 合,加熱該混合物t1時間后(假設雜質不參加反應),冷卻,稱量剩余固體的質量,重復以上操作,依次稱得加熱t1、t2、t3、t4時間后剩余固體的質量,記錄
合,加熱該混合物t1時間后(假設雜質不參加反應),冷卻,稱量剩余固體的質量,重復以上操作,依次稱得加熱t1、t2、t3、t4時間后剩余固體的質量,記錄 數據如下表:
數據如下表:
|
| t1 | t2 | t3 | t4 |
| 剩余固體質量/g | 2.48 | 2.34 | 2.04 | 2.04 |
(1)在________時間后,該樣品中的氯酸鉀已經完全反應 (1分)
(2)完全反應后產生氧氣的質量_______________ (1分)
(3)該樣品中氯酸鉀的質量分數 (4分)
查看答案和解析>>
科目:初中化學 來源: 題型:
過氧化氫溶液可以消毒、殺菌過氧化氫不穩定會自然分解,久置的過氧化氫溶液,其溶質質量分數會變小.某興趣小組為測定實驗室中一瓶久置的過氧化氫溶液中溶質的質量分數,進行如下實驗,測得相關數據如圖所示:
(1)反應生成氧氣的質量為 .
(2)參加反應的過氧化氫的質量為多少克?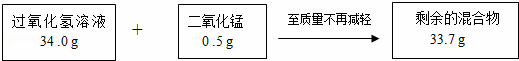
查看答案和解析>>
科目:初中化學 來源: 題型:
航天技術中的火箭推進劑可用醇類為燃料,液態氧為氧化劑,但后者的沸點較低(-183℃),需要額外的隔熱裝置,因而增加了火箭的重量。為了避免此缺點,可用過氧化氫(H2O2)代替液態氧,它具有相對高的沸點和較低的凝固點,而且沒有毒性,和醇反應時也能放出很高的能量。現有一液體推進劑以醇(含碳52%,含氫13%,含氧35%)為燃料,質量分數為90%的過氧化氫作氧化劑,欲使1 kg 該醇燃料完全燃燒,計算需消耗質量分數為90%的過氧化氫的質量。(提示:①醇消耗氧的質量可按它的各元素消耗的氧來計算;②H2O2提供的氧可按2H2O2 2H2O + O2↑來計算)
2H2O + O2↑來計算)
查看答案和解析>>
科目:初中化學 來源: 題型:
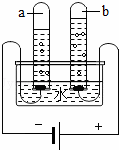
如圖所示是電解水實驗裝置.通電一段時問后,在兩個試管中分別收集到氣體a和氣體b.請回答:
(1)電解水時,將 轉化為化學能.
(2)氣體a為 .
(3)實驗室燃燒氣體a時,首先要 .
(4)水中氫元素和氧元素的質量比是 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com