
| 序號 | KClO3的質量 | 其他物質的質量 | 溫度 | 氧氣的體積 | 反應所需時間 |
| ① | 2.0g | 330℃ | 100mL | t1 | |
| ② | 2.0g | CuO 0.5g | 330℃ | 100mL | t2 |
| ③ | 2.0g | MnO2 0.5g | 330℃ | 100mL | t3 |
| ④ | 2.0g | MnO20.5 g | 380℃ | 100mL | t4 |
分析 (1)如果氧化銅能加快氯酸鉀的分解速率,實驗②比實驗①所用時間小;
(2)根據表格中數據結合控制變量法進行分析實驗對比目的;
(3)根據表格中數據結合控制變量法進行分析;
(4)根據氯酸鉀在二氧化錳做催化劑、380℃時分解生成氯化鉀和氧氣寫出反應的方程式;
(5)根據對照試驗只有一個變量,這個變量為催化劑的顆粒大小設計對照試驗.
解答 解:(1)如果氧化銅能加快氯酸鉀的分解速率,實驗①比實驗②所用時間多,若要確定氧化銅是此反應的催化劑,還需探究反應前后,氧化銅的質量和化學性質不變.
(2)從圖中數據看,KClO3的質量、溫度、氧氣的體積均相同,因此實驗③和實驗②對比的目的是探究氧化銅是否比二氧化錳的催化效果更好;
(3)從圖中數據看,實驗④中控制MnO2的質量為0.5g,若t3>t4,則化學反應快慢與溫度的關系是溫度越高,反應速率越快;
(4)氯酸鉀在二氧化錳做催化劑、380℃時分解生成氯化鉀和氧氣,反應的化學方程式是:2KClO3$\frac{\underline{\;\;\;MnO_{2}\;\;\;}}{380℃}$2KCl+3O2↑.
(5)①取不同顆粒大小的同一催化劑與氯酸鉀以相同質量比充分混合;②分別加熱,測定收集等量氧氣所需時間.
故答案為:(1)>;質量; 化學性質;
(2)探究氧化銅是否比二氧化錳的催化效果更好;
(3)0.5;溫度越高,反應速率越快;
(4)2KClO3$\frac{\underline{\;\;\;MnO_{2}\;\;\;}}{380℃}$2KCl+3O2↑;
(5)①取不同顆粒大小的同一催化劑與氯酸鉀以相同質量比充分混合;②分別加熱,測定收集等量氧氣所需時間.
點評 本題是對不同催化劑對催化效果的探究,明確催化劑只是改變反應的速率,對反應的生成物及生成物的量都沒有影響,本身的質量和化學性質在反應前后不變;并通過表格利用控制變量法進行對比分析得出結論.


 智慧課堂密卷100分單元過關檢測系列答案
智慧課堂密卷100分單元過關檢測系列答案 單元期中期末卷系列答案
單元期中期末卷系列答案科目:初中化學 來源: 題型:選擇題
| A. | 食鹽中的主要成分氯化鈉 | B. | 家用發酵粉的主要成分碳酸氫鈉 | ||
| C. | 食醋中的主要成分醋酸 | D. | 大理石中的主要成分碳酸鈣 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
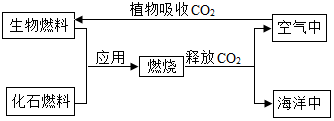
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:填空題
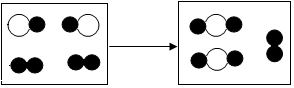 如圖為某化學反應的微觀模擬圖和,“
如圖為某化學反應的微觀模擬圖和,“ ”和“
”和“ ”分別表示兩種不同元素的原子:
”分別表示兩種不同元素的原子:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 唾液中的淀粉酶是一種生物催化劑 | B. | 人體的能量全部由糖類提供 | ||
| C. | 食用加碘鹽可預防甲狀腺腫大 | D. | 蔬菜、水果等富含維生素 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
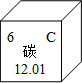 碳在地殼中的含量不高,但由碳元素組成的化合物卻形成了極其龐大的“家族”.
碳在地殼中的含量不高,但由碳元素組成的化合物卻形成了極其龐大的“家族”.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com